题目内容
14.完成以下四个小题:(1)请完成下列各空:
①0.01mol/LCH3COOH溶液的pH>2(填“>”、“=”或“<”)
②0.1mol/LCH3COONa溶液的pH>7(填“>”、“=”或“<”)
(2)观察比较以上二个小题,试猜想证明某酸(HA)是弱电解质的原理有两个一是:测量0.01mol/LHA溶液的pH,若大于2则为弱电解质二是:测量0.1mol/L CH3COONa溶液的pH,若大于7则为弱电解质.
分析 (1)①CH3COOH是弱酸,在水溶液中部分电离;
②CH3COONa属于强碱弱酸盐,弱酸根离子在水溶液中水解显碱性;
(2)证明某酸(HA)是弱电解质的两种较稳妥方法是测定酸的pH或其盐溶液的pH.
解答 解:(1)①CH3COOH是弱酸,在水溶液中部分电离,所以溶液中氢离子浓度小于酸的浓度,所以0.01mol/L CH3COOH溶液的pH>2,故答案为:>;
②CH3COONa属于强碱弱酸盐,醋酸根离子在水溶液中水解显碱性,所以溶液的pH>7,故答案为:>;
(2)证明某酸(HA)是弱电解质的两种较稳妥是测定酸的PH或其盐溶液的pH,因为pH容易测定,
故答案为:测量0.01mol/LHA溶液的pH,若大于2则为弱电解质;测量0.1mol/L CH3COONa溶液的pH,若大于7则为弱电解质.
点评 本题考查了弱电解质的电离,盐类的水解,以及弱电解质的判断方法,题目难度一般.

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目
4.已知SO32-的还原性比I-强.某无色溶液可能含有I-、Fe3+、Na+、SO32-四种离子中的一种或几种,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于该溶液组成的判断正确的是( )
①肯定不含Fe3+;②肯定含I-;③可能含I-;④肯定含SO32-;⑤肯定含Na+;⑥可能含Na+.
①肯定不含Fe3+;②肯定含I-;③可能含I-;④肯定含SO32-;⑤肯定含Na+;⑥可能含Na+.
| A. | ①③④ | B. | ③④⑥ | C. | ①②④ | D. | ①③④⑤ |
9.若阿伏加德罗常数的数值为NA,则下列说法中正确的是( )
| A. | 1 molFe与过量的氯气反应,转移电子的数目为2 NA | |
| B. | 2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA | |
| C. | 1.0L0.1 mol•L-1Na2S溶液中含有的S2-离子数小于0.1NA | |
| D. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA |
6.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 | |
| B. | 碳酸钠溶液与氢氧化钙溶液反应:溶液中产生气泡 | |
| C. | 氢气在空气中燃烧:无色气体燃烧,发出淡蓝色火焰,放热 | |
| D. | 镁条在空气中燃烧:银白色固体燃烧,生成白色固体氧化镁 |
3.下列变化过程中,需要加入氧化剂才能实现的是( )
| A. | Cu→Cu2+ | B. | SO32-→SO2 | C. | Fe2O3→Fe | D. | MnO4-→Mn2+ |
4.设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
| A. | 1.8 g的NH4+离子中含有的电子数为0.1NA | |
| B. | 1mol Na2O2 固体中含离子总数为4NA | |
| C. | 标准状况下,2.24L CCl4所含的共价键数为O.4NA | |
| D. | 常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA |
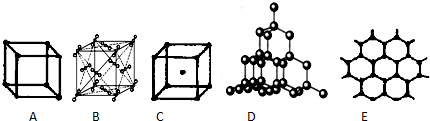
 .一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键
.一定条件下,硫与地壳中含量最多的非金属元素X可组成两种常见的化合物,则X是O,两种化合物均含有的化学键为共价键