题目内容
3.将下列晶体熔化:氢氧化钠、四氯化碳、二氧化硅、氧化钙,需要克服的微粒间的相互作用力依次是:①共价键②离子键③分子间作用力,正确的顺序是( )| A. | ①②②③ | B. | ②①③② | C. | ②③①② | D. | ①①②③ |
分析 离子晶体中含有离子键,原子晶体中含有共价键,分子晶体中含有分子间作用力,根据晶体类型确定熔化晶体时克服的微粒间作用力.
解答 解:NaOH和CaO属于离子晶体,熔化时需要克服的是离子键;
SiO2属于原子晶体,熔化时需要克服的是共价键;
CCl4属于分子晶体,熔化时需要克服的是分子间作用力;所以正确的顺序为:②③①②,
故选C.
点评 本题考查了晶体的类型,明确晶体的构成微粒是解本题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列有关化学用语使用正确的是( )
| A. | 原子核内有8个中子的氧离子:${\;}_{8}^{18}$O | |
| B. | 硫离子的结构示意图: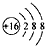 | |
| C. | NH4Cl的电子式: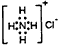 | |
| D. | 二氧化碳的结构式:O-C-O |
18.下列关于有机化合物的结构、性质的叙述正确的是( )
| A. | 乙烯和苯都能使溴水层褪色,褪色的原因相同 | |
| B. | 淀粉、油脂、蛋白质都能水解,且都属于有机高分子化合物 | |
| C. | 蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体 | |
| D. | 乙醇、乙酸均能与NaOH溶液反应,因为分子中均含有官能团“-OH” |
8.下列离子方程式书写正确的是( )
| A. | NH4HCO3溶于少量的浓KOH溶液中:NH4++HCO3-+2OH-═CO32-+NH3↑+2 H2O | |
| B. | 将1mol过氧化钠投入含有1molAlCl3的溶液中:6Na2O2+6H2O+4Al3+═4Al(OH)3↓+3O2↑+12Na+ | |
| C. | NaHSO4溶液中加入Ba(OH)2溶液至溶液呈中性:Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| D. | 将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)6Fe+20 H++5NO3-═3Fe2++3Fe3++5NO↑+10H2O |
15.下列对应的性质描述及方程式解释均正确的是( )
| A. | 苯和溴水在铁作催化剂下发生反应: +Br$\stackrel{Fe}{→}$ +Br$\stackrel{Fe}{→}$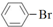 +HBr +HBr | |
| B. | 乙二醛(OHC-CHO)与银氨溶液反应:OHC-CHO+4Ag(NH3)2OH$\frac{\underline{\;\;△\;\;}}{\;}$(NH4)2C2O4+4Ag↓+2H2O+6NH3 | |
| C. | 蔗糖水解生成葡糖糖:C12H22O11+H2O$\underset{\stackrel{稀硫酸}{→}}{△}$2C6H12O6(葡糖糖) | |
| D. | 乙二醇与硬脂酸酯化可以生成硬脂酸甘油酯: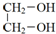 +2C17H35COOH$→_{△}^{浓硫酸}$ +2C17H35COOH$→_{△}^{浓硫酸}$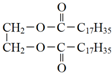 |
6.真菌聚酮(X)具有多种生物活性,一定条件下可分别转化为Y和Z.
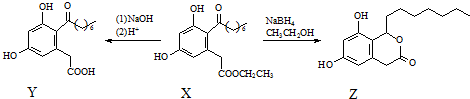
下列说法正确的是( )

下列说法正确的是( )
| A. | X、Y和Z中均不含手性碳原子 | |
| B. | Y能发生氧化、还原、取代、消去反应 | |
| C. | 一定条件下,1 mol X最多能与5 mol H2发生加成反应 | |
| D. | 1 mol Z最多可与含3 mol NaOH的溶液反应 |




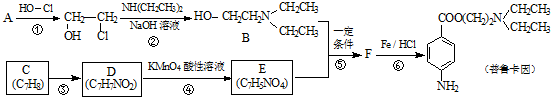
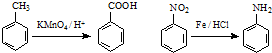
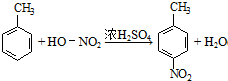 .
.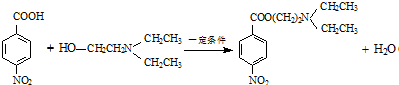 .
.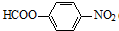 .
.