题目内容
将足量的铜屑加入到100 mL浓度均为2 mol·L-1的HNO3和H2SO4的混合溶液中,充分反应后,转移电子的物质的量为 ( )
A.0.6 mol B.0.8 mol C.0.45 mol D.0.4 mol
C
【解析】
试题分析:100 mL浓度均为2 mol·L-1的HNO3和H2SO4的混合溶液中n(H+)=0.1L×2 mol·L-1+0.1L×2 mol·L-1×2=0.6mol,n(NO3-)=0.1L×2 mol·L-1=0.2mol,根据反应3Cu+2NO3-+8H+=3Cu2++2NO↑+4 H2O可知氢离子不足,所以按氢离子的量进行计算,则生成NO的物质的量是0.6mol/4=0.15mol,所以转移电子的物质的量是0.15mol×3=0.45mol,答案选C。
考点:考查金属与混酸的计算

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 、SO
、SO 、CO
、CO 、NO
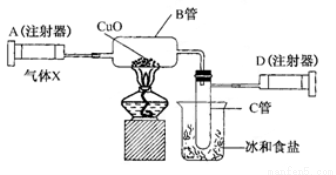
、NO 。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( )
。取200 mL该溶液,分为等体积的两份分别做下列实验。实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224 mL。实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33 g。下列说法正确的是( ) B.二氧化硅的分子式SiO2
B.二氧化硅的分子式SiO2