题目内容
14.对于反应2A2+B2=2A2B,已知A2、B2、A2B的键能如下表| 化学键 | A-A | B=B | A-B |
| 键能kJ/mol | 236 | 406 | 163 |
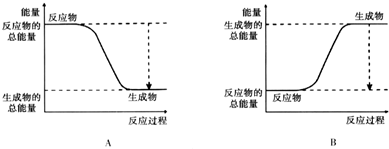
分析 根据△H=反应物的键能总和-生成物的键能总和得到△H的大小,若△H>0,为吸热反应,对应B图,若△H<0,为放热反应,对应A图.
解答 解:△H=反应物的键能总和-生成物的键能总和=(2×236+406-2×2×163)kJ/mol=+226kJ/mol>0,为吸热反应,对应B图,
故答案为:B.
点评 本题考查了化学反应中能量转化的原因,难度不大,根据△H=反应物的键能总和-生成物的键能总和得到△H的大小即可解答.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
4.下列表示物质结构的化学用语或说法中,正确的是( )
| A. | 中子数为8的氮原子:8N | |
| B. | 次氯酸的电子式: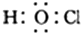 | |
| C. | PCl5分子的每个原子都满足8电子稳定结构 | |
| D. | 用电子式表示NaCl的形成过程: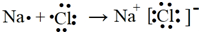 |
5.下列有机物中能使酸性KMnO4溶液褪色,但不能使溴水因发生反应而褪色的是( )
①甲烷 ②乙烯 ③丙炔 ④苯 ⑤甲苯 ⑥乙醇 ⑦乙醛 ⑧乙酸乙酯.
①甲烷 ②乙烯 ③丙炔 ④苯 ⑤甲苯 ⑥乙醇 ⑦乙醛 ⑧乙酸乙酯.
| A. | 只有⑤ | B. | ⑤⑥ | C. | ①④⑧ | D. | ②③⑤⑦ |
2.下列既属于氧化还原反应,又属于吸热反应的是( )
| A. | 铝片与稀盐酸反应 | B. | 氢氧化钡与氯化铵的反应 | ||
| C. | 灼热的碳与水蒸气的反应 | D. | 铝热反应 |
9.下列说法正确的是( )
| A. | 同周期X、Y、Z元素的最高价含氧酸的酸性:HXO4>H2YO4>H3ZO4,则气态氢化物还原性HX<H2Y<ZH3 | |
| B. | 元素R的含氧酸的化学式是H2RO3,则其气态氢化物的化学式就是RH4 | |
| C. | 金属与非金属元素分界线附近的元素是过渡元素 | |
| D. | 物质的量相同的Na+、O2-、NH3三种微粒,一定含有相同的质子 |
6.某周期的第ⅠA族元素的原子序数为x,那么同一周期第ⅢA族元素的原子序数为( )
| A. | 肯定是x+2 | B. | 肯定是x+2或x+8或x+32 | ||
| C. | 肯定是x+2或x+12或x+26 | D. | 肯定是x+2或x+10或x+26 |
3.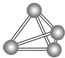 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )
 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )
意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子.N4分子结构如图所示,下列说法正确的是( )| A. | N4分子属于一种新型的化合物 | B. | N4分子中只含有共价键 | ||
| C. | 1 mol N4分子所含共价键数为4NA | D. | N4沸点比P4(白磷)高 |
6.下列说法中正确的是( )
| A. | 已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,则浓硫酸与稀NaOH溶液反应、稀醋酸与稀NaOH溶液反应所测得的中和热都为△H=-57.3kJ/mol | |
| B. | 由C(石墨,s)═C(金刚石,s)△H=+1.9kJ/mol,可知金刚石比石墨稳定 | |
| C. | 在用标准盐酸滴定未知浓度氢氧化钠溶液的实验中,若用待测液润洗锥形瓶,则测定结果偏低(其他操作正确) | |
| D. | 向存在着FeCl3 (黄色)+3KSCN?Fe(SCN)3(血红色)+3KCl平衡体系的溶液中,加少量KCl固体,溶液血红色不发生变化 |