题目内容
13.将足量澄清石灰水加入250ml碳酸钠溶液中,过滤、干燥后得到20g沉淀.(1)写出发生的反应方程式.
(2)求此碳酸钠溶液的物质的量浓度.
(3)若取出这20g沉淀,向其中加入足量的稀盐酸充分反应,求最终产生的气体在标准状况下的体积.
(要求写出计算过程)
分析 (1)发生的反应方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)20g沉淀为碳酸钙,根据方程式计算碳酸钠的物质的量,再根据c=$\frac{n}{V}$计算;
(2)发生反应:CaCO3+2HCl=CaCl2+CO2↑+H2O,据此计算生成二氧化碳的体积.
解答 解:(1)发生的反应方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,答:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(2)令碳酸钠的物质的量为x mol,则:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
1mol 100g
xmol 20g
1mol:xmol=100g:20g
解得x=0.2
碳酸钠的物质的量浓度=$\frac{n}{V}$=$\frac{0.2mol}{0.25L}$=0.8mol/L,
答:碳酸钠的物质的量浓度为0.8mol/L;
(3)设标况下生成二氧化碳的体积为V L,则:
CaCO3+2HCl=CaCl2+CO2↑+H2O
100g 22.4L
20g V L
100g:20g=22.4L:V L
解得V=4.48,
答:标况下生成二氧化碳的体积为4.48L.
点评 本题考查化学方程式的有关计算、物质的量的计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
4.下列物质中属于弱电解质的是( )
| A. | 醋酸 | B. | 氨 | C. | 碳酸氢钠 | D. | NaOH溶液 |
8.下列离子方程式书写正确的是( )
| A. | 硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag | |
| B. | 氧化钠投入水中发生反应:O2-+H2O=2OH- | |
| C. | 向澄清石灰水中通入足量二氧化碳:OH-+CO2=HCO3- | |
| D. | 金属铁溶于稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
18.根据原子结构及元素周期律的知识,下列推断正确的是( )
| A. | 同主族元素含氧酸的酸性随核电荷数的增加而减弱 | |
| B. | Cl-、S2-、Ca2+、K+半径逐渐减小 | |
| C. | 核外电子排布相同的微粒化学性质也相同 | |
| D. | ${\;}_{17}^{35}$Cl与${\;}_{17}^{37}$Cl得电子能力相同 |
5.下列过程有热量放出的是( )
| A. | 断开氢气中的H-H键 | B. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 | ||
| C. | C与H2O(g)反应 | D. | Na与H2O反应 |

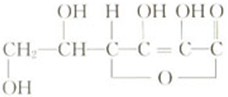 维生素C的结构式如下,
维生素C的结构式如下,