题目内容
17.下列关于有机物的叙述不正确的是( )| A. | 鉴别己烷、己烯和乙醇,可用溴水 | |
| B. | 乙烯和植物油均能使溴的四氯化碳溶液褪色,且反应原理相同 | |
| C. | 甲苯苯环上的一个氢原子被-C3H6Cl取代,形成的同分异构体有9种 | |
| D. | 1mol分子式为C18H26O5的酯完全水解生成lmol 羧酸和2mol乙醇,该羧酸分子式为C14H18O5 |
分析 A.己烷不溶于水,己烯与溴水发生加成反应,乙醇易溶于水;
B.乙烯和植物油都含有碳碳双键;
C.-C3H6Cl与甲基有邻、间、对三种,且-C3H6Cl有5种同分异构体;
D.1mol该酯完全水解可得到1mol羧酸和2mol乙醇,则说明酯中含有2个酯基,结合酯的水解特点以及质量守恒定律判断.
解答 解:A.己烷不溶于水,己烯与溴水发生加成反应,乙醇易溶于水,现象不同,可鉴别,故A正确;
B.乙烯和植物油都含有碳碳双键,都可与溴发生加成反应,故B正确;
C.-C3H6Cl在甲苯苯环上位置有3种情况,-C3H6Cl中碳链异构为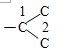 和
和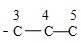 ,数字编号为Cl的位置,因此-C3H6Cl异构情况为5种,故同分异构体的种类为:3×5=15,故C错误;
,数字编号为Cl的位置,因此-C3H6Cl异构情况为5种,故同分异构体的种类为:3×5=15,故C错误;
D.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,说明酯中含有2个酯基,设羧酸为M,则反应的方程式为C18H26O5+2H2O=M+2C2H6O,由质量守恒可知M的分子式为C14H18O5,故D正确.
故选C.
点评 本题考查有机物的结构与性质及推断,为高频考点,侧重考查学生的分析能力,把握官能团与性质的关系为解答的关键,易错点为C,注意同分异构体的判断,难度中等.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
7.BaCl2常用作分析试剂,也常直接用于制造钡盐以及电子、仪表、冶金等工业.我国目前比较成熟的生产BaCl2•xH2O的工艺是以重晶石(主要成分BaSO4,杂质为Fe2O3)、无烟煤粉和盐酸为原料生产,流程如图所示(部分产物已略去).

(1)写出BaCl2的电子式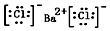 .
.
(2)“还原焙烧”时,使过量的无烟煤粉和重晶石粉混合物在高温下发生反应,该反应的化学方程式为BaSO4+4C$\frac{\underline{\;焙烧\;}}{\;}$BaS+4CO↑.
(3)“盐酸浸”得到的是氯化钡粗液,其中残余的含硫化合物会影响产品质量,必须通过鼓入热空气吹除.鼓入热空气能有效去杂的原理是升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去.
(4)生产过程中所产生的尾气含有毒性较高的H2S,为防止环境污染,必须进行吸收处理,下列不可行的吸收液是BC.
A.CuSO4溶液B.浓硫酸C.NaHS溶液D.氨水
(5)随着工艺条件的不同,产品BaCl2•xH2O中的x数值有所不同.产品检验部门通常采用的操作是:Ⅰ称取样品a g;Ⅱ充分加热;Ⅲ置于干燥器中冷却;Ⅳ称量质量为b g.由此可得出x=$\frac{208(a-b)}{18b}$(请写出计算表达式).
(6)工业检测MgCl2•xH2O中的x值时不用以上加热法,而多采用沉淀滴定法,其原因是(用化学方程式表示)MgCl2•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2HCl+(x-1)H2O.沉淀滴定的测定步骤为:称取0.5000g待测产品,用适量硝酸溶解,滴加指示剂,用AgNO3标准溶液滴定.
根据上表数据分析,该滴定可选用Na2CrO4作指示剂.使用该指示剂时,判断滴定达到终点的现象是当滴入最后一滴AgNO3溶液出现砖红色沉淀,放置30s砖红色不消失.

(1)写出BaCl2的电子式
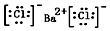 .
.(2)“还原焙烧”时,使过量的无烟煤粉和重晶石粉混合物在高温下发生反应,该反应的化学方程式为BaSO4+4C$\frac{\underline{\;焙烧\;}}{\;}$BaS+4CO↑.
(3)“盐酸浸”得到的是氯化钡粗液,其中残余的含硫化合物会影响产品质量,必须通过鼓入热空气吹除.鼓入热空气能有效去杂的原理是升高温度可降低H2S的溶解度,利于吹出;升高温度,利于使H2S氧化成S沉淀除去.
(4)生产过程中所产生的尾气含有毒性较高的H2S,为防止环境污染,必须进行吸收处理,下列不可行的吸收液是BC.
A.CuSO4溶液B.浓硫酸C.NaHS溶液D.氨水
(5)随着工艺条件的不同,产品BaCl2•xH2O中的x数值有所不同.产品检验部门通常采用的操作是:Ⅰ称取样品a g;Ⅱ充分加热;Ⅲ置于干燥器中冷却;Ⅳ称量质量为b g.由此可得出x=$\frac{208(a-b)}{18b}$(请写出计算表达式).
(6)工业检测MgCl2•xH2O中的x值时不用以上加热法,而多采用沉淀滴定法,其原因是(用化学方程式表示)MgCl2•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2HCl+(x-1)H2O.沉淀滴定的测定步骤为:称取0.5000g待测产品,用适量硝酸溶解,滴加指示剂,用AgNO3标准溶液滴定.
| AgCl | AgI | Ag2CrO4 | |
| Ksp | 2×10-10 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 黄 | 砖红 |
8.化学与生产、生活、社会发展等息息相关,下列说法正确的是( )
| A. | “可燃冰”被认为是21世纪新型洁净的能源,但大量开发和使用会诱发海底地质灾害,还会加重温室效应 | |
| B. | 碘元素被誉为“智力元素”,KI、KIO3、I2都可作碘盐的添加剂 | |
| C. | 硅橡胶无毒无味、耐高温又耐低温,可制成人造心脏,它属于无机非金属材料 | |
| D. | “雾霾天气”“温室效应”“光化学烟雾”的形成都与氮的氧化物无关 |
5.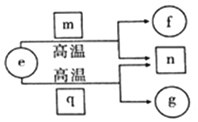 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
 短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )
短周期元素X、Y、Z、W的原子序数依次增加,且Y、W为同主族元素.e、f、g分别是元素 Y、X、W的单质;m、n、q分别是由元素X、Y、W与元素Z组成的二元化合物,常温下的 状态依次为液态、气态、固态.上述物质的转化关系如图所示.下列说法错误的是( )| A. | 原子半径的大小:W>Z>X | |
| B. | 简单氢化物的沸点:W>Y>Z | |
| C. | 元素Y、Z、W形成的单质不止一种 | |
| D. | 元素Y、Z、W与元素X均能形成18e-的分子 |
12.以下有关有机物的应用或说法正确的是( )
| A. | 葡萄糖、蔗糖均可发生银镜反应 | |
| B. | 硫酸铵和乙酸铅均能使蛋白质发生变性 | |
| C. | 乙炔和乙醛均可合成聚合物 | |
| D. | 淀粉和油脂都是能发生水解反应的高分子化合物 |
2.两种气态烃的混合物共2.24L(标准状况下),完全燃烧后得3.36L(标准状况下)二氧化碳和3.6g的水.下列说法中,正确的是( )
| A. | 混合气体中一定含有甲烷 | B. | 混合气体中一定含有乙烯 | ||
| C. | 混合气体中一定含有甲烷和乙烯 | D. | 混合气体中一定含有乙烷 |
18.下列关于NaHCO3的说法正确的是( )
| A. | 俗名是苏打或纯碱 | B. | 同温度时的溶解度比Na2CO3大 | ||
| C. | 与盐酸反应时比Na2CO3快 | D. | 热稳定性强,受热难以分解 |
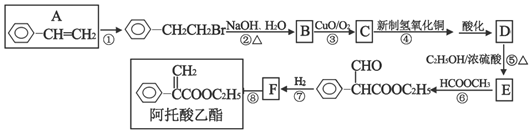
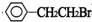 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$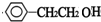 +NaBr.反应③的方程式
+NaBr.反应③的方程式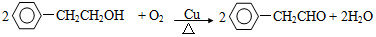 .
.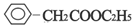 ;
;