题目内容
13.胶体区别于其他分散系的本质特征是( )| A. | 加热会聚沉 | B. | 分散质颗粒大小在1-100nm之间 | ||
| C. | 胶体微粒不能透过半透膜 | D. | 产生丁达尔现象 |
分析 胶体区别于其他分散系的本质特征是分散质微粒直径的大小不同,据此解答.
解答 解:分散系按照分散质粒度大小可以分为溶液、胶体与浊液,分散质粒度依次小于1nm,介于1-100nm,大于100nm,胶体区别于其它分散系的本质特征是胶体粒子直径在1-100nm之间,
故选:B.
点评 本题考查了胶体的本质特征,较简单,明确分散系划分依据是解题关键,注意对基础知识的积累.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案
相关题目
3.已知反应COCl2(g)?CO(g)+Cl2(g)△H>0.当反应达到平衡时,下列措施:①升温 ②恒容通入稀有气体 ③增加COCl2的浓度 ④减压 ⑤加催化剂 ⑥恒压通入稀有气体,能提高此反应的化学反应速率的是( )
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ①③⑤ |
4.以乙烯为原料生产环氧乙烷,经典的方法是氯代乙醇法,包括以下两步反应:
①CH2=CH2+Cl2+H2O→CICH2CH2OH+HCI
②ClCH2CH2OH+HCl+Ca(OH)2→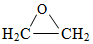 +CaCl2+2H2O
+CaCl2+2H2O
总的反应可表示为:
CH2=CH2+Cl2+Ca(OH)2→ +CaCl2+H2O
+CaCl2+H2O
现代石油化式采用银作催化剂,可一步完成例:
2CH2=CH2+O2 $\stackrel{Ag}{→}$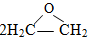
经典的生产工艺的原子利用率是( )
①CH2=CH2+Cl2+H2O→CICH2CH2OH+HCI
②ClCH2CH2OH+HCl+Ca(OH)2→
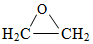 +CaCl2+2H2O
+CaCl2+2H2O总的反应可表示为:
CH2=CH2+Cl2+Ca(OH)2→
 +CaCl2+H2O
+CaCl2+H2O现代石油化式采用银作催化剂,可一步完成例:
2CH2=CH2+O2 $\stackrel{Ag}{→}$

经典的生产工艺的原子利用率是( )
| A. | 12.7% | B. | 25.4% | C. | 50.8% | D. | 76.2% |
8.关于阿斯匹林的作用叙述中不正确的是( )
| A. | 杀菌消炎 | B. | 解热镇痛 | C. | 防止心脏病发作 | D. | 提高免疫力 |
18.下列有关叙述正确的是( )
| A. | 在NaHS溶液中滴人少量CuCl2溶液,产生黑色沉淀,HS-水解程度增大,pH增大 | |
| B. | 常温下,由于HCO3-水解显碱性,所以饱和NaHCO3溶液显碱性 | |
| C. | 泡沫灭火器是利用Al2(SO4)3溶液与饱和NaHCO3溶液混合产生气体 | |
| D. | 配制氯化铝溶液时,先将氯化铝溶于浓硫酸,再加水稀释 |
5.用 NA 表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | T℃1 L pH=6 的纯水中含 10-6 NA个 OH | |
| B. | 6.0 g SiO2 晶体中含有 0.1 NA 个 SiO2分子 | |
| C. | 标准状况下,22.4 L HF 所含电子数为 10NA | |
| D. | 标准状况下,22.4 L 氧气作氧化剂时转移电子数一定为 4NA |
9.下列离子方程式中,正确的是( )
| A. | 向NaOH溶液中加入少量Mg(HCO3)2溶液:2OH-+Mg2+═Mg(OH)2↓ | |
| B. | 向足量NaHSO4溶液中逐渐滴入Ba(HCO3)2溶液:2HCO3-+Ba2++2H++SO42-═BaSO4↓+2H2O+2CO2↑ | |
| C. | 酸性KMnO4溶液与H2O2反应:2MnO4-+10H++3H2O2═2Mn2++3O2↑+8H2O | |
| D. | 向Fe(NO3)3溶液中加入过量HI溶液:2Fe3++2I-═2Fe2++I2 |
10.某溶液可能存在Na+、Ba2+、Mg2+、Fe3+、Br-、CO32-、Cl-等离子,某学生进行下列实验:取少量原溶液,测得溶液呈强碱性,在其中滴加足量氯水,有无色无味气体产生,溶液仍为无色.关于该原溶液的推测正确的是( )
| A. | 溶液中可能存在Mg2+和Fe3+ | B. | 溶液中可能存在Br-和Cl- | ||
| C. | 溶液可能存在Ba2+和Cl- | D. | 溶液中一定存在Na+和CO32- |