题目内容
13.已知碳酸二级电离较偏铝酸的电离容易,而石炭酸的电离介于碳酸的一级电离与二级电离之间.下面的推论正确的是①⑤:①将CO2通入偏铝酸钠溶液中,溶液变浑浊,并生成碳酸钠或碳酸氢钠;②将CO2通入C6H5ONa溶液中,离子反应式为CO2+H2O+2C6H5O-→2C6H5OH+CO32-;
③HCO3-在溶液中既能与AlO2-又能与Al3+反应,且都发生双水解;④往含有大量CO32-的溶液中加入C6H5OH得到澄清溶液,放出CO2气体;⑤向Al(OH)3的混浊液中加入Na2CO3溶液得不到澄清溶液;⑥相同温度,相同浓度的Na2CO3、C6H5ONa、NaHCO3、NaAlO2的稀溶液PH依次增大.
分析 已知碳酸二级电离较偏铝酸的电离容易,而石炭酸的电离介于碳酸的一级电离与二级电离之间,则酸性:H2CO3>C6H5OH>HCO3->Al(OH)3,结合酸性强的能制备酸性弱的来分析解答.
解答 解:已知碳酸二级电离较偏铝酸的电离容易,而石炭酸的电离介于碳酸的一级电离与二级电离之间,则酸性:H2CO3>C6H5OH>HCO3->Al(OH)3,
①H2CO3和HCO3-的酸性均大于Al(OH)3,将CO2通入偏铝酸钠溶液中,溶液生成Al(OH)3沉淀,二氧化碳少量时生成碳酸钠,二氧化碳过量时生成碳酸氢钠,故正确;
②已知酸性:H2CO3>C6H5OH>HCO3-,将CO2通入C6H5ONa溶液中生成苯酚和碳酸氢钠,离子反应式为CO2+H2O+C6H5O-→C6H5OH+HCO3-,故错误;
③HCO3-的酸性大于Al(OH)3,HCO3-在溶液中与AlO2-反应是利用强酸制备弱酸的原理,HCO3-与Al3+反应是发生双水解,故错误;
④已知酸性:H2CO3>C6H5OH>HCO3-,往含有大量CO32-的溶液中加入C6H5OH得到澄清溶液,生成碳酸氢根离子,不能放出CO2气体,故错误;
⑤酸性:HCO3->Al(OH)3,Al(OH)3与Na2CO3溶液不反应,所以向Al(OH)3的混浊液中加入Na2CO3溶液得不到澄清溶液,故正确;
⑥相同温度,相同浓度盐溶液,对应的酸的酸性越弱,其盐的水解能力越强,其盐溶液的pH越大,则NaHCO3、C6H5ONa、Na2CO3、NaAlO2的稀溶液PH依次增大,故错误.
故答案为:①⑤.
点评 本题考查了强酸制弱酸原理的应用、盐的水解原理的应用,题目难度不大,侧重于考查学生对基本原理的应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列各组离子能在指定环境下大量共存的是( )
| A. | C(HCO3-)=0.1mol/L的溶液中:NH4+、Al3+、Cl-、NO3- | |
| B. | 室温下,PH=2的溶液中:Fe2+、SO42-、Na+、NO3- | |
| C. | 无色透明的溶液中:NH4+、Cl-、NO3-、Fe3+ | |
| D. | 使红色石蕊试纸变蓝的溶液中:SO32-、Na+、CO32-、K+ |
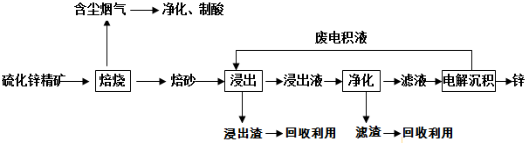
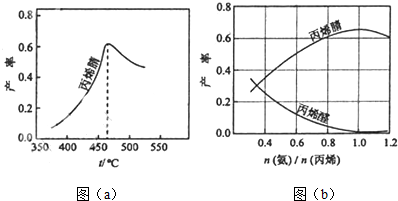
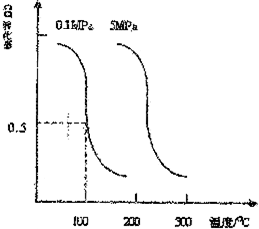 研究和开发CO2 和CO的创新利用是环境保护和资源利用的双赢的课题.
研究和开发CO2 和CO的创新利用是环境保护和资源利用的双赢的课题.