题目内容
1. 研究和开发CO2 和CO的创新利用是环境保护和资源利用的双赢的课题.
研究和开发CO2 和CO的创新利用是环境保护和资源利用的双赢的课题.ⅠCO可用于合成甲醇.在压强为0.1Mpa条件下,在体积为bL的密闭容器中充入amolCO和2amolH2,在催化剂作用下合成甲醇;
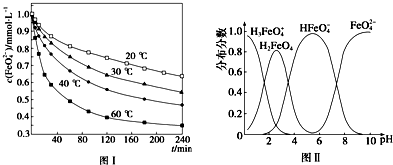
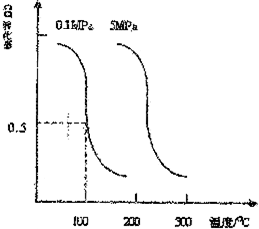
CO(g)+2H2(g)?CH3OH(g)平衡时CO的转化率与温度,压强的关系如图:
(1)100℃时,该反应的平衡常数:K=$\frac{{b}^{2}}{{a}^{2}}$;(用a、b的代数式表示).若一个可逆反应的平衡常数K值很 大,对此反应的说法正确的是:C(填序号)
A.该反应使用催化剂意义不大;
B.该反应发生将在很短时间内完成;
C.该反应达到平衡时至少有一种反应物百分含量很小;
D.反应物的转化率一定高:
(2)在温度和容积不变的情况下,再向平衡体系中充入amolCO,2amolH2,达到平衡时CO转化率增大(填“增大”,“不变”或“减小”,下同)平衡常数:不变.
(3)在某温度下,向一容积不变的密闭容器中充入2.5molCO,7.5molH2,反应生成CH3OH(g),达到平衡时,CO转化率为90%,此时容器内压强为开始时的压强0.55倍.
Ⅱ某温度条件下,若将CO2(g)和H2(g)以体积比1:4混合,在适当压强和催化剂作用下可制得甲烷,己知:
$\left.\begin{array}{l}$CH4(g)+2O2(g)=CO2(g)+2H2O(1)△H=-890.3KJ/mol H2(g)+1/2O2(g)=H2O(1)△H=-285.8KJ/mol则CO2(g)和H2(g)反应生成液态水的热化学方程式为:CO2(g)+4H2(g)=CH4(g)+2H2O(l)△H=-252.9kJ•mol-1.
分析 I.(1)化学平衡常数K=$\frac{c(C{H}_{3}OH)}{c(CO){c}^{2}({H}_{2})}$,根据CO的转化率,利用三段式计算出平衡时各组分的物质的量,进而求出平衡时各组分的浓度,代入平衡常数计算;
可逆反应的平衡常数越大,说明反应进行的程度越大,不能说明反应速率快慢、不能说明该反应在通常条件下一定可以发生、不能说明反应是吸热还是放热;
(2)在温度和容积不变的情况下,再向平衡体系中充入a mol CO(g)、2a mol H2(g),等效为在原平衡的基础上增大一倍压强,平衡向正反应移动;
化学平衡常数只受温度影响,与浓度无关,温度不变,平衡常数不变;
(3)计算参加反应的CO的物质的量,利用差量法计算平衡时反应混合物的物质的量变化量,进而计算平衡时总的物质的量,利用恒温恒容下,压强之比等于物质的量之比解答;
II.根据盖斯定律书写目标热化学方程式.
解答 解:I.(1)100℃,平衡时CO的转化率为0.5,所以参加反应的CO的物质的量为0.5amol.
CO(g)+2H2(g)?CH3OH(g);
开始(mol):a 2a 0
变化(mol):0.5a a 0.5a
平衡(mol):0.5a a 0.5a
所以平衡时,CO的浓度为$\frac{0.5amol}{bL}$=$\frac{a}{2b}$mol/L,H2的浓度为$\frac{a}{b}$mol/L,CH3OH的浓度为$\frac{0.5amol}{bL}$=$\frac{a}{2b}$mol/L,100℃时该反应的平衡常数k═$\frac{\frac{a}{2b}}{\frac{a}{2b}×(\frac{a}{b})^{2}}$=$\frac{{b}^{2}}{{a}^{2}}$,
A.可逆反应的平衡常数很大,说明反应进行的程度很大,不能说明该反应在通常条件下一定可以发生,该反应可能需要催化剂才可以进行,故A错误;
B.可逆反应的平衡常数很大,说明反应进行的程度很大,不能说明该条件下反应速率很快,故B错误;
C.可逆反应的平衡常数很大,说明反应进行的程度很大,反应达平衡时至少有一种反应物的百分含量很小,故C正确;
D.可逆反应的平衡常数很大,说明反应进行的程度很大,不能说明该反应是吸热还是放热,故D错误,
故答案为:$\frac{{b}^{2}}{{a}^{2}}$;C;
(2)在温度和容积不变的情况下,再向平衡体系中充入a mol CO(g)、2a mol H2(g),等效为在原平衡的基础上增大一倍压强,平衡向正反应移动,CO的转化率增大,化学平衡常数只受温度影响,与浓度无关,温度不变,平衡常数不变,
故答案为:增大;不变;
(3)参加反应的CO的物质的量为2.5mol×90%=2.25mol,则:
CO(g)+2H2(g)?CH3OH(g) 物质的量减少△n
1 2
2.25mol 4.5mol
故平衡时总的物质的量为2.5mol+7.5mol-4.5mol=5.5mol,恒温恒容下压强之比等于物质的量之比,故平衡时容器内压强为开始时压强的$\frac{5.5mol}{2.5mol+7.5mol}$=0.55倍,
故答案为:0.55;
II.已知:①CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1=-890.3kJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H2=-285.8kJ•mol-1,
利用盖斯定律,将②×4-①可得:CO2(g)+4H2(g)=CH4(g)+2H2O(l)△H=4×(-285.8kJ•mol-1)-(-890.3kJ•mol-1)=-252.9kJ•mol-1,
故答案为:CO2(g)+4H2(g)=CH4(g)+2H2O(l)△H=-252.9kJ•mol-1.
点评 本题考查化学平衡图象、化学平衡有关计算、化学平衡常数、影响化学平衡的因素、热化学方程式书写,是对知识的综合运用,应加强平时知识的积累,难度中等.

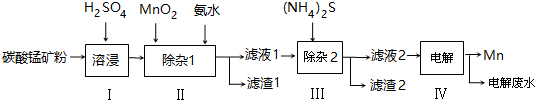
已知25℃,部分物质的溶度积常数如表:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)则滤渣1的主要成分为Fe(OH)3(填化学式).已知MnO2的作用为氧化剂,则得到该成分所涉及的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;Fe3++3NH3﹒H2O=Fe(OH)3↓+3NH4+.
(3)步骤Ⅲ中,所加(NH4)2S的浓度不宜过大的原因是若(NH4)2S的浓度过大,产生MnS沉淀,造成产品损失.
(4)滤液2中,c(Co2+):c(Ni2+)=5:1.
(5)将质量为a kg的碳酸锰矿经上述流程处理后得到单质Mn b kg.若每一步都进行完全,滤渣1为纯净物,质量为c kg,则原碳酸锰矿中MnCO3的质量分数为$\frac{(b-\frac{c}{107}×\frac{1}{2}×55)×\frac{115}{55}}{a}$×100%.(用含a、b、c的式子表达,无需化简)
| A. | 1mol•L-1NaCl溶液含有NA个Na+ | |
| B. | 1mol Cl2与足量的铝反应,转移的电子数为3NA | |
| C. | 1 mol Na 与足量O2 反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 | |
| D. | 铁和酸反应,放出标准状况下的22.4L气体,转移的电子数必为2NA |
 按要求填空:
按要求填空: