题目内容
12.现有73g HCl气体.若阿伏加德罗常数的数值用NA表示,则:(1)该气体的物质的量为2mol.
(2)该气体所含原子总数为4NA个.
(3)该气体在标准状况下的体积为44.8L.
(4)该气体溶于1L水中(水的密度为1g•cm-3),其溶液中溶质的质量分数为6.8%.
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为$\frac{2}{V}$mol•L-1.
分析 (1)根据n=$\frac{m}{M}$计算HCl的物质的量;
(2)原子物质的量为HCl的2倍,再根据N=nNA计算;
(3)根据V=nVm计算HCl的体积;
(4)根据m=ρV计算水的质量,进而计算溶液质量,再根据质量分数定义计算;
(5)根据c=$\frac{n}{V}$计算所得溶液物质的量浓度.
解答 解:(1)气体的摩尔质量为36.5g•mol-1,73g HCl气体的物质的量=$\frac{73g}{36.5g/mol}$=2mol,故答案为:2;
(2)原子物质的量为2mol×2=4mol,故含有原子数目为4NA,故答案为:4NA;
(3)标况下,HCl的体积=2mol×22.4L/mol=44.8L,故答案为:44.8;
(4)1L水的质量为1000mL×1g/mL=1000g,溶液质量分数=$\frac{73g}{1000g+73g}$×100%=6.8%,故答案为:6.8%;
(5)溶于水后形成VL溶液,所得溶液物质的量浓度=$\frac{2mol}{VL}$=$\frac{2}{V}$mol/L,故答案为:$\frac{2}{V}$.
点评 本题考查物质的量有关计算,难度不大,掌握以物质的量为中心的计算公式.

练习册系列答案
 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
3.相同温度下,体积均为0.5L的两个恒容密闭容器中发生可逆反应:X2(g)+3Y2(g)?2XY3(g)△H=-92.6kJ•mol-1实验测得反应在起始、达到平衡时的有关数据如下表所示:
(1)达平衡时,②容器中XY3的物质的量浓度为2mol/L
(2)列式计算①中反应的平衡常数$\frac{4}{27}$(计算结果用分数表示))
(3)容器②中反应达到平衡时放出(填“吸收”或“放出”)的热量为Q=9.26kJ
(4)若容器①体积为0.40L,则达平衡时放出的热量大于(填“大于”“等于”“小于”)46.3kJ.
| 容器编号 | 起始时各物质物质的量(mol) | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热 46.3kJ |
| ② | 0.6 | 1.8 | 0.8 | Q (Q>0) |
(2)列式计算①中反应的平衡常数$\frac{4}{27}$(计算结果用分数表示))
(3)容器②中反应达到平衡时放出(填“吸收”或“放出”)的热量为Q=9.26kJ
(4)若容器①体积为0.40L,则达平衡时放出的热量大于(填“大于”“等于”“小于”)46.3kJ.
20.下列离子方程式书写正确的是( )
| A. | 氯气通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 盐酸滴入澄清石灰水中:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ | |
| D. | 铜与硝酸银溶液反应:Cu+2Ag+═Cu2++2Ag |
7.除去下列物质中的少量杂质(括号内的物质为杂质),所选出的试剂或方法不正确的是( )
| A. | CO2(SO2):饱和碳酸氢钠溶液 | B. | N2(O2):灼热的铜网 | ||
| C. | Al2O3(SiO2):NaOH溶液 | D. | Na2CO3固体(NaHCO3):加热 |
4.足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、NO、N2O的混合气体,这些气体与X L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入5mol•L-1NaOH溶液至Cu2+恰好完全沉淀,消耗NaOH溶液的体积是160mL,则X的值为( )
| A. | 2.24 | B. | 3.36 | C. | 4.48 | D. | 1.12 |
2.如图下列仪器,可以直接加热的是( )
| A. | 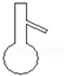 | B. |  | C. |  | D. |  |

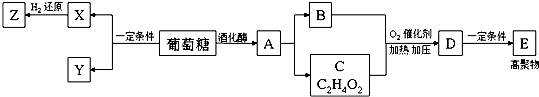
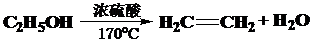 .
.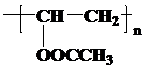 .
. .
.