题目内容
下列实验及离子方程式书写不正确的是( )
| A、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| B、氯化亚铁溶液与过氧化钠2:1反应:6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+6Na++2Fe3+ |
| C、三氯化铁溶液中通入过量硫化氢气体:2Fe3++H2S=2Fe2++S↓+2H+ |
| D、在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.酸性高锰酸钾溶液具有强氧化性,能够氧化氯离子,不能用浓盐酸酸化,可以用稀硫酸;
B.氯化亚铁与过氧化钠按照2:1反应,亚铁离子恰好被氧化成铁离子,氢氧根离子不足,铁离子有剩余;
C.铁离子具有氧化性,能够氧化硫化氢,反应生成亚铁离子、硫单质;
D.氢氧化钙足量,离子方程式按照碳酸氢镁的组成书写,反应生成氢氧化镁沉淀、碳酸钙沉淀和水.
B.氯化亚铁与过氧化钠按照2:1反应,亚铁离子恰好被氧化成铁离子,氢氧根离子不足,铁离子有剩余;
C.铁离子具有氧化性,能够氧化硫化氢,反应生成亚铁离子、硫单质;
D.氢氧化钙足量,离子方程式按照碳酸氢镁的组成书写,反应生成氢氧化镁沉淀、碳酸钙沉淀和水.
解答:
解:A.用浓盐酸酸化的KMnO4溶液与H2O2反应,由于氯离子具有还原性,能够被酸性高锰酸钾溶液氧化成氯气,无法证明H2O2具有还原性,应该用稀硫酸酸化,故A错误;
B.氯化亚铁溶液与过氧化钠2:1反应,亚铁离子恰好被氧化成铁离子,反应的离子方程式为:6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+6Na++2Fe3+,故B正确;
C.三氯化铁溶液中通入过量硫化氢气体,铁离子将硫化氢氧化成硫单质,反应的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,故C正确;
D.碳酸氢镁溶液中加入足量Ca(OH)2溶液,反应生成氢氧化镁沉淀、碳酸钙沉淀和水,反应的离子方程式为:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O,故D正确;
故选A.
B.氯化亚铁溶液与过氧化钠2:1反应,亚铁离子恰好被氧化成铁离子,反应的离子方程式为:6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+6Na++2Fe3+,故B正确;
C.三氯化铁溶液中通入过量硫化氢气体,铁离子将硫化氢氧化成硫单质,反应的离子方程式为:2Fe3++H2S=2Fe2++S↓+2H+,故C正确;
D.碳酸氢镁溶液中加入足量Ca(OH)2溶液,反应生成氢氧化镁沉淀、碳酸钙沉淀和水,反应的离子方程式为:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O,故D正确;
故选A.
点评:本题考查了离子方程式的正误判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
下列在酸性溶液中能大量共存的离子组是( )
A、Fe2+、NO
| ||
| B、K+、Cl-、SO42-、Al3+ | ||
C、S2-、Na+、NH4+、NO
| ||
D、SO42-、K+、NO
|
 在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是( )
在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是( )| A、①②③④ | B、①③④ |
| C、①②④ | D、②③④ |
下列分散系不属于胶体的是( )
| A、淀粉溶液 | B、有色玻璃 |
| C、食盐水 | D、油水 |
下列对于硝酸的认识,正确的是( )
| A、浓硝酸和稀硝酸都具有强氧化性 |
| B、铜和稀硝酸的反应属于置换反应 |
| C、在铜与浓硝酸的反应中,硝酸只体现氧化性,没有体现酸性 |
| D、可用铝或铁制容器盛装稀硝酸 |

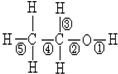 乙醇分子中的化学键如右图,在不同反应中断键不同:和金属钠反应
乙醇分子中的化学键如右图,在不同反应中断键不同:和金属钠反应