题目内容
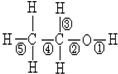 乙醇分子中的化学键如右图,在不同反应中断键不同:和金属钠反应
乙醇分子中的化学键如右图,在不同反应中断键不同:和金属钠反应考点:乙醇的化学性质
专题:有机物的化学性质及推断
分析:根据乙醇的性质,结合反应物与产物的结构判断.有机反应重在掌握反应的机理即清楚断键与成键位置.
乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键;
乙醇在铜催化下与O2反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢.
乙醇与与金属钠反应生成乙醇钠和氢气,断开的羟基上的氢氧键;
乙醇在铜催化下与O2反应生成乙醛和水,断开的是羟基上的氢氧键和与羟基所连的碳的氢.
解答:
解:乙醇与金属钠反应生成乙醇钠和氢气:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故乙醇断键的位置为:①;乙醇在铜催化下与O2反应生成乙醛和水:2CH3CH2OH+O
2CH3CHO+2H2O,故乙醇断键的位置为①和③,
故答案为:①,2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,①③.
| Cu或Ag |
| △ |
故答案为:①,2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,①③.
点评:本题考查乙醇的性质,题目难度不大.掌握反应的机理是解题的关键,注意化学方程式的书写.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
相关题目
NaOH溶液中通入Cl2的离子反应方程式为( )
| A、H2O+Cl2=HCl+HClO |
| B、2OH-+Cl2=Cl-+ClO-+H2O |
| C、NaOH+Cl2=Na++Cl-+ClO-+H2O |
| D、OH-+H2O+Cl2=Cl-+HClO |
下列实验及离子方程式书写不正确的是( )
| A、用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
| B、氯化亚铁溶液与过氧化钠2:1反应:6Fe2++3Na2O2+6H2O=4Fe(OH)3↓+6Na++2Fe3+ |
| C、三氯化铁溶液中通入过量硫化氢气体:2Fe3++H2S=2Fe2++S↓+2H+ |
| D、在碳酸氢镁溶液中加入足量Ca(OH)2溶液:Mg2++2HCO3-+2Ca2++4OH-═Mg(OH)2↓+2CaCO3↓+2H2O |
下列各组有机物中,无论以何种比例混合,只要二者的物质的量之和不变,完全燃烧时消耗的氧气及生成的水的物质的量也不变的是( )
| A、C2H2和C6H6 |
| B、C2H6和C2H5OH |
| C、C2H4和C2H6O |
| D、C6H6和C7H6O2 |
 请回答下列涉及的几个有关油脂的问题.
请回答下列涉及的几个有关油脂的问题.