题目内容
某液态卤代烷RX(R是烷基,X是某种卤原子)的密度是a g?cm-3.RX可以与稀碱发生水解反应生成ROH(能跟水互溶)和HX.为了测定RX的相对分子质量,拟定的实验步骤如下:
①准确量取该卤代烷b mL,放入锥形瓶中.
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应.
③反应完成后,冷却溶液,加稀硝酸酸化,滴加过量AgNO3溶液得到白色沉淀.
④将沉淀过滤、洗涤、干燥后称重,得到固体c g.
回答下列问题:
(1)装置中长玻璃管的作用是 .
(2)该卤代烷中所含卤素的名称是 ,判断依据是 .
(3)如R为乙基,则RX与KOH醇溶液反应的方程式为:
(4)如果在步骤③中,加HNO3的量不足,没有将溶液酸化,则步骤④测得的c值
A.偏大 B.偏小 C.不变 D.大小不定.
①准确量取该卤代烷b mL,放入锥形瓶中.
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应.
③反应完成后,冷却溶液,加稀硝酸酸化,滴加过量AgNO3溶液得到白色沉淀.
④将沉淀过滤、洗涤、干燥后称重,得到固体c g.
回答下列问题:
(1)装置中长玻璃管的作用是
(2)该卤代烷中所含卤素的名称是
(3)如R为乙基,则RX与KOH醇溶液反应的方程式为:
(4)如果在步骤③中,加HNO3的量不足,没有将溶液酸化,则步骤④测得的c值
A.偏大 B.偏小 C.不变 D.大小不定.
考点:测定有机物分子的元素组成
专题:实验题
分析:本题涉及的实验原理是:RX+KOH→ROH+KX,KX+AgNO3=AgX↓+KNO3.
(1)RX熔沸点较低,加热时易挥发,据此确定长导管的作用;
(2)含有卤素原子的离子中,能和硝酸银反应生成白色沉淀的只能是氯离子,据此来回答判断;
(3)卤代烃在强碱的醇溶液作用下会发生消去反应得到烯烃、氯化钠和水;
(4)在溶液中,AgOH会转化为Ag2O沉淀,根据转化关系来计算回答.
(1)RX熔沸点较低,加热时易挥发,据此确定长导管的作用;
(2)含有卤素原子的离子中,能和硝酸银反应生成白色沉淀的只能是氯离子,据此来回答判断;
(3)卤代烃在强碱的醇溶液作用下会发生消去反应得到烯烃、氯化钠和水;
(4)在溶液中,AgOH会转化为Ag2O沉淀,根据转化关系来计算回答.
解答:
解:(1)因RX熔沸点较低,加热时易挥发,所以装置中长导管的作用是防止卤代烃挥发或冷凝回流,故答案为:冷凝回流,提高原料利用率;
(2)因为所得AgX沉淀为白色,能和硝酸银反应生成白色沉淀的只能是氯化银沉淀,所以卤代烃中含有氯元素,故答案为:氯;滴加过量AgNO3溶液,得白色沉淀;
(3)R为乙基,则CH3CH2Cl与KOH醇溶液反应的方程式为:CH3CH2Cl+KOH
CH2═CH2↑+KCl+H2O,故答案为:CH3CH2Cl+KOH
CH2═CH2↑+KCl+H2O;
(4)若加HNO3的量不足,未将溶液酸化,则沉淀中还有AgOH转化为Ag2O沉淀,由于氢氧化银和氧化银的影响,故测得的c值将偏大,故答案为:A.
(2)因为所得AgX沉淀为白色,能和硝酸银反应生成白色沉淀的只能是氯化银沉淀,所以卤代烃中含有氯元素,故答案为:氯;滴加过量AgNO3溶液,得白色沉淀;
(3)R为乙基,则CH3CH2Cl与KOH醇溶液反应的方程式为:CH3CH2Cl+KOH
| 醇 |
| △ |
| 醇 |
| △ |
(4)若加HNO3的量不足,未将溶液酸化,则沉淀中还有AgOH转化为Ag2O沉淀,由于氢氧化银和氧化银的影响,故测得的c值将偏大,故答案为:A.
点评:本题考查有机物分子式的确定,难度中等,注意卤素离子的检验方法,属于综合知识的考查题.

练习册系列答案
相关题目
在恒温下,密闭容器中的可逆反应:2SO3(气)?2SO2(气)+O2(气)可用来确定该反应已经达到平衡状态的是( )
| A、反应容器内,压强不随时间改变 |
| B、单位时间消耗1molSO3同时生成1molSO2 |
| C、单位时间消耗1molSO3同时消耗1molSO2 |
| D、容器内混合气体的总质量不发生变化 |
下列说法正确的是( )
A、按系统命名法,化合物 的名称为2,4-二乙基-6-丙基辛烷 的名称为2,4-二乙基-6-丙基辛烷 |
B、DDT的结构简式为 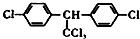 ,分子中最多有14个碳原子共平面 ,分子中最多有14个碳原子共平面 |
| C、醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物 |
D、结构片段为 的高聚物,是其单体通过缩聚反应生成 的高聚物,是其单体通过缩聚反应生成 |
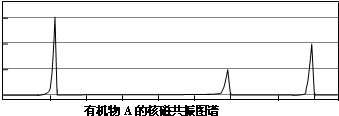
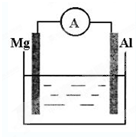 如图所示,组成一个原电池.
如图所示,组成一个原电池.