题目内容
20.由铝、锌、铜、银和稀硫酸,可以组成原电池的总数为( )| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
分析 该原电池中,电解质溶液为稀硫酸,正、负极电极材料活泼性必须不同,且负极和电解质溶液能自发的进行氧化还原反应,据此进行分析.
解答 解:铝,锌,铜,银这四种金属的活泼性不同,但能和稀硫酸自发的进行氧化还原反应的金属只有铝和锌,所以负极材料必须含有铝或锌中的一种,
则以下几种情况的电极与稀硫酸可组成的原电池:①铝和锌、②铝和铜、③铝和银、④锌和铜、⑤锌和银,
所以组成原电池的总数为5种,
故选B.
点评 本题考查了原电池工作原理,题目难度不大,明确原电池工作原理为解答关键,判断正负极材料时要根据原电池的形成条件来确定,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
11.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系不正确的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. | 饱和Ca(OH)2溶液 |
| B | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | Ca(ClO)2溶液 |
| C | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. | Ca(OH)2溶液 |
| D | 通入NH3,溶液变浑浊.继续通NH3至过量,浑浊消失. | NaAlO2溶液 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法中、错误的是( )
| A. | 化学反应必然伴随发生能量变化 | |
| B. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| C. | 人体运动所消耗的能量与化学反应无关 | |
| D. | 能量变化是化学反应的基本特征之一 |
15.下列表示物质结构的化学用语正确的是( )
| A. | 8个中子的碳原子的核素符号:12C | B. | NaCl 的电子式  | ||
| C. | Cl-离子的结构示意图: | D. | CO2的结构式:O=C=O |
5.短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
| R | |||
| T | Q | W | |
| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | T的氧化物属于两性氧化物 | |
| D. | W的氧化物对应的水化物一定是强酸 |
12.下列化学反应的离子方程式正确的是( )
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 铁与稀HNO3反应:Fe+2H+=═Fe2++H2↑ | |
| C. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| D. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-═Fe3++2H20+NO↑ |
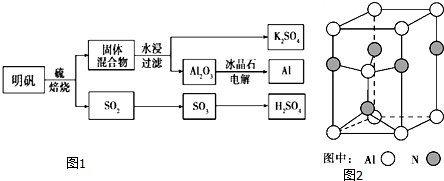
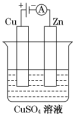 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在100kPa时,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃),N2H4完全燃烧的热化学方程式是N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-642kJ/mol.
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在100kPa时,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃),N2H4完全燃烧的热化学方程式是N2H4(l)+2H2O2(l)=N2(g)+4H2O(l)△H=-642kJ/mol.