题目内容
1.铁在地壳中的含量约占 5%左右.铁矿石的种类很多,重要的有磁铁矿石、赤铁矿石等.红热的铁能跟水蒸气反应,则其反应的化学方程式为3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2.其生成黑色的物质溶于酸后,加入KSCN,见不到血红色产生,其原因是Fe3O4+8H+═Fe2++2Fe3++4H2O、Fe+2Fe3+=3Fe2+(用离子方程式解释).再向此溶液中加入足量氢氧化钠,生成沉淀颜色会由白色迅速变为灰绿色最后变为红褐色,写出此变化的化学方程为4Fe(OH)2+2H2O+O2=4Fe(OH)3.分析 红热的铁能与水蒸气发生反应,生成Fe3O4和一种可燃性气体,可燃气体为氢气;黑色的物质溶于酸后,加入KSCN,见不到血红色产生,说明溶液中无铁离子,可能是黑色固体物质中含有单质铁;亚铁离子与氢氧化钠反应生成氢氧化亚铁,氢氧化亚铁不稳定,很容易被氧化成氢氧化铁.
解答 解:红热的铁能与水蒸气发生反应,生成Fe3O4和氢气,反应方程式为:3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,黑色的物质溶于酸后,加入KSCN,见不到血红色产生,说明溶液中无亚铁离子,可能是黑色固体物质中含有单质铁,反应方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O,Fe+2Fe3+=3Fe2+;
再向此溶液中加入足量氢氧化钠,亚铁离子与NaOH反应生成白色沉淀氢氧化亚铁,氢氧化亚铁不稳定,易被空气中氧气氧化,则沉淀颜色会由白色迅速变为灰绿色最后变为红褐色,反应的化学方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3,
故答案为:3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;Fe3O4+8H+═Fe2++2Fe3++4H2O;Fe+2Fe3+=3Fe2+;4Fe(OH)2+2H2O+O2=4Fe(OH)3.
点评 本题考查了化学方程式的书写及应用,题目难度不大,明确发生反应实质为解答关键,注意掌握铁及其化合物性质,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 mL水中含有的分子数目约为1.24NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 23g钠在氧气中完全燃烧失去电子数为0.5NA | |
| D. | 常温常压下的33.6L氯气与56g铁充分反应,转移电子数为3NA |
12.在强酸性无色溶液中,下列各组离子可能大量共存的是( )
| A. | Cu2+、NH4+、SO42-、Cl-、 | B. | Na+、K+、CO32-、Cl- | ||
| C. | K+、Fe2+、MnO4-、Cl- | D. | Na+、K+、NO3-、Cl- |
9.下列实验设计、操作或实验现象不合理的是( )
| A. | 实验室制取乙炔时,用饱和食盐水代替蒸馏水,以得到平稳的气流 | |
| B. | 除去苯中的少量苯酚:加入适量NaOH溶液,振荡、静置、分液 | |
| C. | 检验甲酸中是否混有乙醛,可向样品中加入足量NaOH溶液以中和甲酸后,再做银镜反应实验或与新制Cu(OH)2共热的实验 | |
| D. | 液态溴乙烷中加入稀NaOH溶液共煮几分钟,然后加入足量稀硝酸,再加入AgNO3溶液检验溴乙烷中是否含有溴元素 |
16.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L 水蒸气中含有3NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是NA |
13.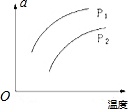 在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
 在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )
在容积一定的密闭容器中发生可逆反应X(g)+3Y(g)?nZ(g);△H>0,平衡移动关系如图所示.下列说法正确的是( )| A. | a可能表示混合气体的密度 | |
| B. | 若n=3,p1>p2,则a可表示Y的质量分数 | |
| C. | 若n=3,p1>p2,则a可表示Y的转化率 | |
| D. | a不可能表示混合气体的平均摩尔质量 |
10.下列物质之间的转化不能通过一步反应实现的是( )
| A. | Fe(OH)2→Fe(OH)3 | B. | FeCl3→FeCl2 | C. | Al2O3→Al(OH)3 | D. | Na2CO3→NaHCO3 |
11.下列各物质的晶体中,晶体类型相同的是( )
| A. | CCl4和NaCl | B. | NaI和I2 | C. | CO2和C60 | D. | Mg和H2 |