题目内容
欲除去下列物质中混入的少量杂质(括号内物质为杂质),正确的是( )
| A、乙酸乙酯(乙酸):加入适量乙醇,充分反应 |
| B、乙醇(水):加入新制生石灰,蒸馏 |
| C、乙烷(乙烯):加入适量H2,适当条件下进行反应 |
| D、乙醇(乙酸):加入金属钠,蒸馏 |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:A.乙酸乙酯中混有新杂质乙醇;
B.CaO与水反应后增大与乙醇的沸点差异;
C.乙烷中混有新杂质氢气;
D.二者均与Na反应.
B.CaO与水反应后增大与乙醇的沸点差异;
C.乙烷中混有新杂质氢气;
D.二者均与Na反应.
解答:
解:A.乙酸乙酯中混有新杂质乙醇,不能除杂,应选饱和碳酸钠溶液、分液来除杂,故A错误;
B.CaO与水反应后增大与乙醇的沸点差异,然后蒸馏可除杂,故B正确;
C.乙烷中混有新杂质氢气,不能除杂,应选溴水、洗气可除杂,故C错误;
D.二者均与Na反应,不能除杂,应选NaOH、蒸馏除杂,故D错误;
故选B.
B.CaO与水反应后增大与乙醇的沸点差异,然后蒸馏可除杂,故B正确;
C.乙烷中混有新杂质氢气,不能除杂,应选溴水、洗气可除杂,故C错误;
D.二者均与Na反应,不能除杂,应选NaOH、蒸馏除杂,故D错误;
故选B.
点评:本题考查混合物分离、提纯方法的选择和应用,为高频考点,把握物质的性质及性质差异、常见混合物分离方法为解答的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2⑤CO2和C2H2 ⑥SiO44-和SO42-.
| A、全部 | B、除①④⑥以外 |
| C、③④⑤⑥ | D、②⑤⑥ |
下列关于杂化轨道的叙述中,正确的是( )
| A、分子中的中心原子通过SP2杂化轨道成键时,该分子一定为平面三角形 |
| B、CH4分子中有四个完全相同的sp3-s6键 |
| C、杂化轨道只用于形成6键 |
| D、杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾 |
假设厨房里的食用油不慎混入较多水分,采用下列何种方法可以正确分离( )
| A、过滤 | B、蒸馏 | C、分液 | D、萃取 |
下列说法不正确的是( )
| A、粘有油脂的试管可以用热的纯碱溶液洗涤 |
| B、石油的分馏、裂化、裂解都是化学变化 |
| C、食醋中含有乙酸,乙酸可由乙醇氧化得到 |
| D、煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 |
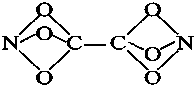 某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )
某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )| A、该分子的分子式为CNO3 |
| B、分子中既含极性键又含非极性键 |
| C、C、N的化合价分别为+4、+3 |
| D、该物质为高分子化合物 |
乙醇分子中不同的化学键如图所示,关于乙醇有关性质的说法不正确的是( )
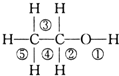

| A、和金属钠反应键①断裂 |
| B、在铜催化下和O2反应键①④断裂 |
| C、乙醇与金属钠反应比水与金属钠反应缓慢 |
| D、钠与乙醇反应时,钠熔化成一个小球在乙醇表面不断的游动 |
下面有关氯化铯晶体的叙述中,不正确的是( )
| A、1mol氯化铯中有N 个CsCl分子 |
| B、氯化铯晶体中,每个Cs+周围距离相等的Cs+共有6个 |
| C、氯化铯晶体中,每个Cs+周围紧邻8个C1- |
| D、平均每个Csc1晶胞中有1个Cs+、1个C1- |
| E、平均每个Csc1晶胞中有1个Cs+、1个C1- |
关于反应K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O的有关叙述中,正确的是( )
| A、KCl中含有35Cl |
| B、生成物Cl2的相对分子质量为73.3 |
| C、该反应转移的电子数为6e- |
| D、氧化剂和还原剂的物质的量之比为1:6 |