��Ŀ����
ij�о�С����CaCl2��H2Ϊԭ�ϣ��Ʊ�+1��Ca�Ļ����������ֲ�����ֻ�����ֻ�������ң���Ԫ����ɷ���������������иơ���Ԫ�ص����������ֱ�Ϊ52.36%��46.33%���������ҵ�ˮ��Һ�����ԣ���ش��������⣺
��1�����о�С���Ƿ�ɹ��Ƶ�+1��Ca�Ļ���� ����ǡ������Ļ�ѧʽ�� ��
��2������ˮ��Ӧ�ɵ�H2���仯ѧ����ʽ�� ����Ӧ������Һ���ᾧ�ɵõ�һ�־��壬�仯ѧʽΪCaCl2?xCa��OH��2?12H2O��Ϊȷ��x��ֵ�������ʵ�鷽�� ��
��3���ڼ��������£��ҵ�ˮ��Һ��Ũ����MnO2��Ӧ�����ӷ���ʽ�� ���ҵ�ˮ��Һ��Fe��Ӧ���õ���Һ���ȶ����������Һ�Ĵ�ʩ�� ��
��4����д��һ������Ϊ���ܵõ�CaCl�Ļ�ѧ����ʽ����CaCl2Ϊԭ�ϣ� ��
��1�����о�С���Ƿ�ɹ��Ƶ�+1��Ca�Ļ����
��2������ˮ��Ӧ�ɵ�H2���仯ѧ����ʽ��
��3���ڼ��������£��ҵ�ˮ��Һ��Ũ����MnO2��Ӧ�����ӷ���ʽ��
��4����д��һ������Ϊ���ܵõ�CaCl�Ļ�ѧ����ʽ����CaCl2Ϊԭ�ϣ�
���㣺����ʵ�鷽�������,�Ʊ�ʵ�鷽�������
ר�⣺ʵ�������
��������1������������������иơ���Ԫ�ص����������ֱ�Ϊ52.36%��46.33%������һ��Ԫ�أ����ݷ�Ӧ��Ԫ���غ�֪����һ��Ԫ��Ϊ��Ԫ�أ������ԭ�ӡ���ԭ�Ӻ���ԭ�Ӹ���֮��=
��
��
=1��1��1���������ҵ�ˮ��Һ�����ԣ���Ϊ�Ȼ��⣻
��2����ˮ��Ӧ����������ͬʱ�����Ȼ��ơ��������ƣ���ѧʽΪCaCl2?xCa��OH��2?12H2O�����ʣ���������ˮ������̼���ƣ��õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
�������x��
��3���������̺�Ũ����֮����ȷ�Ӧ���������Ȼ��̡�ˮ�Լ��������Ȼ������ױ�����Ϊ�Ȼ�����������ˮ�⣬�ݴ˻ش�
��4���Ȼ��Ʒ������Ϸ�Ӧ����CaCl���Ȼ��������������������ԭ����
| 52.36% |
| 40 |
| 46.33 |
| 35.5 |
| 1-52.36%-46.33% |
| 1 |
��2����ˮ��Ӧ����������ͬʱ�����Ȼ��ơ��������ƣ���ѧʽΪCaCl2?xCa��OH��2?12H2O�����ʣ���������ˮ������̼���ƣ��õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
| 2n(Ca2+)-n(Cl-) |
| n(Cl-) |
��3���������̺�Ũ����֮����ȷ�Ӧ���������Ȼ��̡�ˮ�Լ��������Ȼ������ױ�����Ϊ�Ȼ�����������ˮ�⣬�ݴ˻ش�
��4���Ȼ��Ʒ������Ϸ�Ӧ����CaCl���Ȼ��������������������ԭ����
���
�⣺��1������������������иơ���Ԫ�ص����������ֱ�Ϊ52.36%��46.33%������һ��Ԫ�أ����ݷ�Ӧ��Ԫ���غ�֪����һ��Ԫ��Ϊ��Ԫ�أ������ԭ�ӡ���ԭ�Ӻ���ԭ�Ӹ���֮��=
��
��
=1��1��1����ѧʽΪ��CaHCl�����ܳɹ��Ƶ�+1��Ca�Ļ������Ԫ�صĻ��ϼ���+2�ۣ�
�ʴ�Ϊ����CaHCl��
��2��CaHCl��ˮ��Ӧ����������ͬʱ�����Ȼ��ơ��������ƣ���Ӧ����ʽΪ��2CaHCl+2H2O=CaCl2+Ca��OH��2+2H2������ѧʽΪCaCl2?xCa��OH��2?12H2O�����ʣ���������ˮ������̼���ƣ��õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
�������xֵ��
�ʴ�Ϊ��2CaHCl+2H2O=CaCl2+Ca��OH��2+2H2����ȡ������ϡHNO3�ܽ��ֳɶ��ȷݣ�����һ�ݼ���Na2CO3��Һ���õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
�������xֵ��
��3���������̺�Ũ����֮����ȷ�Ӧ���������Ȼ��̡�ˮ�Լ�������ʵ���ǣ�2Cl-+MnO2+4H+
Mn2++Cl2��+2H2O���Ȼ������ױ�����Ϊ�Ȼ������������۷�ֹ�����������Ȼ�������ˮ�⣬Ӧ����FeCl2��Һ�����ԣ�
�ʴ�Ϊ������FeCl2��Һ�����ԣ����������۷�ֹ������
��4���Ȼ��Ʒ������Ϸ�Ӧ����CaCl���Ȼ��������������������ԭ������Ӧ����ʽΪ��Ca+CaCl2=2CaCl���ʴ�Ϊ��Ca+CaCl2=2CaCl��
| 52.36% |
| 40 |
| 46.33 |
| 35.5 |
| 1-52.36%-46.33% |
| 1 |
�ʴ�Ϊ����CaHCl��
��2��CaHCl��ˮ��Ӧ����������ͬʱ�����Ȼ��ơ��������ƣ���Ӧ����ʽΪ��2CaHCl+2H2O=CaCl2+Ca��OH��2+2H2������ѧʽΪCaCl2?xCa��OH��2?12H2O�����ʣ���������ˮ������̼���ƣ��õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
| 2n(Ca2+)-n(Cl-) |
| n(Cl-) |
�ʴ�Ϊ��2CaHCl+2H2O=CaCl2+Ca��OH��2+2H2����ȡ������ϡHNO3�ܽ��ֳɶ��ȷݣ�����һ�ݼ���Na2CO3��Һ���õ�CaCO3���������غ����n��Ca2+������һ�ݼ���AgNO3��Һ���õ�AgCl���������غ����n��Cl-������x=
| 2n(Ca2+)-n(Cl-) |
| n(Cl-) |
��3���������̺�Ũ����֮����ȷ�Ӧ���������Ȼ��̡�ˮ�Լ�������ʵ���ǣ�2Cl-+MnO2+4H+
| ||
�ʴ�Ϊ������FeCl2��Һ�����ԣ����������۷�ֹ������
��4���Ȼ��Ʒ������Ϸ�Ӧ����CaCl���Ȼ��������������������ԭ������Ӧ����ʽΪ��Ca+CaCl2=2CaCl���ʴ�Ϊ��Ca+CaCl2=2CaCl��
���������⿼�������ʼ�ķ�Ӧ����ȷ���ʵ������ǽⱾ��ؼ������ʾ�����;����һ������ʵ�鷽��������⣬�ѶȽϴ�

��ϰ��ϵ�д�
�����Ŀ
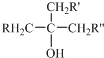 �е�-OH���ܱ�������
�е�-OH���ܱ�������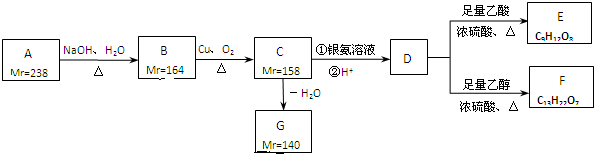
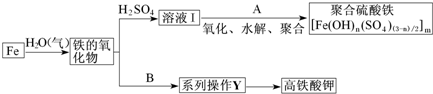
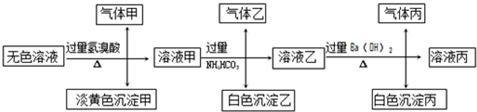
 ��ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ��ݴ˻ش��������⣺
��ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص������Լ���ǩ�ϵIJ������ݣ��ݴ˻ش��������⣺