题目内容
18. 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制的图如图,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制的图如图,则曲线a、b、c、d所对应的实验组别可能是( )| 组别 | 盐酸的浓度(mol/L) | 温度(℃) | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 块状 |
| 4 | 2.5 | 30 | 粉末状 |
| A. | 4-2-3-1 | B. | 1-2-3-4 z | C. | 3-4-2-1 | D. | 1-2-4-3 |
分析 由图象可知,时间t越小反应用的时间越少,反应速率越快,则反应速率为a>b>c>d,然后根据表中数据结合温度、接触面积、浓度对反应速率的影响进行分析.
解答 解:由图象可知,t越小用反应需要的时间越少,反应速率越快,则反应速率为a>b>c>d,由表中数据可知,实验1、2、3中,3中的温度高于1、2,且1的HCl浓度最低,则3中反应速率大于1、2,即3>2>1,2、4中,4的接触面积大,则反应速率4>2,但3和4无法比较,所以反应速率为3>4>2>1.
故选C.
点评 本题考查反应速率的影响因素,把握图象和表格数据的分析是解答的关键,注重学生知识迁移应用能力的考查,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
8.下列化学用语表达正确的是( )
| A. | 丙烯的球棍模型: | B. | 乙醇的比例模型: | ||
| C. | 乙烯的结构简式:CH2 | D. | 羟基的电子式: |
6.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | B. | ClO3-的空间构型为平面三角形 | ||
| C. | SF6中有6对完全相同的成键电子对 | D. | SiF4和SO3的中心原子均为sp2杂化 |
13.沸腾时只需克服范德华力的液体物质是( )
| A. | 水 | B. | 酒精 | C. | 氨水 | D. | CH3Cl |
3.对化学反应的速率和限度的叙述正确的是( )
| A. | 增加某一反应物的用量一定能够加快该反应的速率 | |
| B. | 化学反应的限度是不可改变的 | |
| C. | 化学反应进行的时间越长该反应的限度越大 | |
| D. | 化学反应达到限度时,正逆反应速率相等 |
10.下表是元素周期表的一部分,请按要求回答有关问题:
(1)表中化学性质最不活泼的元素的原子结构示意图为: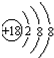 ;
;
(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应的水化物反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)元素④与元素⑦形成的化合物中的化学键类型是离子键,写出该化合物的电子式: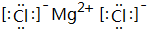 ;
;
(4)①②⑥⑦四种元素的最高价氧化物对应的水化物中酸性最弱的是H2CO3(填化学式);
(5)元素③与元素⑩两者核电荷数之差是26;
(6)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的元素是:②(填序号);
(7)④⑤⑥⑦四种元素的简单离子的半径由大到小的顺序为:S2->Cl->Mg2+>Al3+(填化学式).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
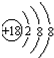 ;
;(2)表中能形成两性氢氧化物的元素是Al(用元素符号表示),写出该元素的单质与⑨的最高价氧化物对应的水化物反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)元素④与元素⑦形成的化合物中的化学键类型是离子键,写出该化合物的电子式:
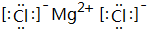 ;
;(4)①②⑥⑦四种元素的最高价氧化物对应的水化物中酸性最弱的是H2CO3(填化学式);
(5)元素③与元素⑩两者核电荷数之差是26;
(6)气态氢化物能与其最高价氧化物对应的水化物反应生成盐的元素是:②(填序号);
(7)④⑤⑥⑦四种元素的简单离子的半径由大到小的顺序为:S2->Cl->Mg2+>Al3+(填化学式).
8.下列说法中正确的是( )
| A. | 由于分子间作用力的存在,因而CO2在加热条件下不易发生分解 | |
| B. | 非金属原子间不可能形成离子化合物 | |
| C. | 在PCl3分子中各原子都达到8电子稳定结构 | |
| D. | 离子化合物中可能存在共价键,共价化合物中也可能存在离子键 |