题目内容
2.某研究性学习小组利用下面的装置自制Zn-O2燃料电池,步骤如下:
Ⅰ.利用电解装置(如图1,A、B均为石墨棒),在多孔的石墨棒上吸附一定量的氧气.
Ⅱ.取出吸附有氧气的石墨棒,用导线将石墨棒、锌板和小灯泡连接,并将石墨棒和锌板插入KNO3溶液中,组装成Zn-O2燃料电池(如图2),使灯泡发光.
(1)电解水的装置中,产生氧气的电极是B(填“A”或“B”).
(2)Zn-O2燃料电池正极的电极反应式是O2+4e-+2H2O=4OH-,该电池放电时溶液中的NO3-向负极移动(填“正”或“负”).
(3)如果Zn-O2燃料电池的锌电极质量减少0.13g,那么电解池中产生氢气在标准状况下的体积至少为44.8mL.
分析 (1)电解水的装置中,氢氧根离子在阳极放电;
(2)原电池中正极发生还原反应,阴离子向负极移动;
(3)根据转移电子守恒:2Zn~~O2~~~2H2.
解答 解:(1)电解水的装置中,氢氧根离子在阳极放电,所以产生氧气的电极是B,故答案为:B;
(2)原电池中正极是氧气发生还原反应,电极反应式为:O2+4e-+2H2O=4OH-,该电池放电时溶液中的NO3-向负极移动,故答案为:O2+4e-+2H2O=4OH-;负;
(3)根据转移电子守恒:2Zn~~O2~~~2H2
65×2g 44.8L
0.13g V(H2)
$\frac{65×2g}{0.13g}=\frac{44.8L}{V({H}_{2})}$
解之得:V(H2)=44.8mL,
故答案为:44.8.
点评 本题考查电化学知识,理解这类题的关键是理解原电池原理,注意教材知识的灵活运用是解题的关键,难度不大.

练习册系列答案
相关题目
13.下列变化中,不属于化学变化的是( )
| A. | SO2使品红溶液褪色 | B. | 氯水使有色布条褪色 | ||
| C. | H2O2 使某些颜料褪色 | D. | 活性炭使红墨水褪色 |
10.关于铝热反应,下列说法不正确的是( )
| A. | 该反应是吸热反应 | B. | 铝热剂是混合物 | ||
| C. | 可以利用该反应焊接铁轨 | D. | 该反应需在高温条件下进行 |
7.下列物质中,既含有离子键,又含有非极性共价键的是( )
| A. | HCl | B. | KOH | C. | CaCl2 | D. | Na2O2 |
14.东汉时,《神龙本草经》记载“石胆…能化铁为铜”.“石胆”或叫“胆矾”,成分是五水硫酸铜(CuSO4•5H2O).下列说法不正确的是( )
| A. | 记载中的反应属于置换反应 | B. | CuSO4溶液呈中性 | ||
| C. | 记载中L含了湿法炼铜的原理 | D. | 每生成1mol铜转移2mol电子 |
11.下列离子方程式正确的是( )
| A. | 盐酸与氢氧化钠溶液反应:H++OH-=H2O | |
| B. | 铜与稀硫酸反应:Cu+2H+=Cu2++H2↑ | |
| C. | 碳酸钙与稀盐酸反应:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| D. | 硫酸铜溶液与氢氧化钡溶液反应:SO${\;}_{4}^{2-}$+Ba2+=BaSO4↓ |
4.下列关于材料的说法错误的是( )
| A. | 羊毛的主要成分是纤维素 | B. | 塑料属于合成材料 | ||
| C. | 普通玻璃属于硅酸盐材料 | D. | 不锈钢属于合金 |
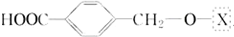 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生. .
. (其中两种).
(其中两种). 为主要原料制备
为主要原料制备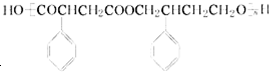 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: .
.