��Ŀ����
4��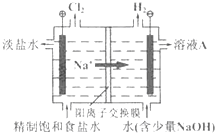 �ȼҵ�Ե�⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ����ͼ�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ�������������գ�
�ȼҵ�Ե�⾫�Ʊ���ʳ��ˮ�ķ�����ȡ�������������ռ���ȵĺ������ε�ϵ�л�����Ʒ����ͼ�����ӽ���Ĥ�����ʳ��ˮ��ʾ��ͼ��ͼ�е����ӽ���Ĥֻ����������ͨ�������������գ���1��д����ⱥ��ʳ��ˮ�����ӷ���ʽ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-��
��2����ҺA��������NaOH��
��3�����ʱ�����������������Һ��pH��2��3���û�ѧƽ���ƶ�ԭ���������������Cl2��ˮ��Ӧ��Cl2+H2O?HCl+HClO������HCl��Ũ��ʹƽ�������ƶ�������Cl2��ˮ�е��ܽ⣬������Cl2���ݳ���
��4��KClO3���ԺͲ��ᣨH2C2O4�������ᷴӦ���ɸ�Ч������ɱ����ClO2��������CO2��KHSO4�����ʣ�д���÷�Ӧ�Ļ�ѧ����ʽ��2KClO3+H2C2O4+2H2SO4=2ClO2��+2CO2��+2KHSO4+2H2O��
��5����֪��
H2SO3 Ka1=1.54��10-2 Ka2=1.02��10-7
HClO Ka=2.95��10-8
H2CO3 Ka1=4.3��10-7 Ka2=5.6��10-11
�����£�0.1mol/L NaClO��Һ��pH����0.1mol/L Na2SO3��Һ��pH����ѡ����ڡ�����С�ڡ����ڡ�����Ũ�Ⱦ�Ϊ0.1mol/L ��Na2SO3��Na2CO3�Ļ����Һ�У�SO32-��CO32-��HSO3-��HCO3-Ũ�ȴӴ�С��˳��Ϊc��SO32-����c��CO32-����c��HCO3-����c��HSO3-����
���� ����ͼ֪����ⱥ��ʳ��ˮʱ���ұߵ缫����������������Һ��ˮ�õ�����������ͬʱ����NaOH������AΪNaOH��
��1���ö��Ե缫��ⱥ��ʳ��ˮʱ�������������ӷŵ�����������������ˮ�õ����������������������ӣ�
��2��AΪNaOH��
��3����������ˮ�������ᣬ������ˮ�ķ�Ӧ�ǿ��淴Ӧ�������������������ܽ⣻
��4�����ݷ�Ӧ�����������д����ʽ��
��5����ĵ���ƽ�ⳣ��Խ���������Ӧ���������ˮ��̶�ԽС����ͬŨ�ȵ�������ҺpHԽС��
��� �⣺����ͼ֪����ⱥ��ʳ��ˮʱ���ұߵ缫����������������Һ��ˮ�õ�����������ͬʱ����NaOH������AΪNaOH��
��1���ö��Ե缫��ⱥ��ʳ��ˮʱ�������������ӷŵ�����������������ˮ�õ����������������������ӣ���ط�ӦʽΪ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-���ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-��
��2��ͨ�����Ϸ���֪��AΪNaOH���ʴ�Ϊ��NaOH��
��3����������ˮ�������ᣬ������ˮ�ķ�Ӧ�ǿ��淴Ӧ�������������������ܽ⣬�������������ݳ����ʴ�Ϊ��Cl2��ˮ��Ӧ��Cl2+H2O?HCl+HClO������HCl��Ũ��ʹƽ�������ƶ�������Cl2��ˮ�е��ܽ⣬������Cl2���ݳ���
��4�����ݷ�Ӧ�����������д����ʽΪ2KClO3+H2C2O4+2H2SO4=2ClO2��+2CO2��+2KHSO4+2H2O���ʴ�Ϊ��2KClO3+H2C2O4+2H2SO4=2ClO2��+2CO2��+2KHSO4+2H2O��
��5����ĵ���ƽ�ⳣ��Խ���������Ӧ���������ˮ��̶�ԽС����ͬŨ�ȵ�������ҺpHԽС��
���ݵ���ƽ�ⳣ��֪������H2SO3��H2CO3��HSO3-��HClO��HCO3-�����������ˮ��̶�CO32-��ClO-��SO32-��HCO3-��HSO3-��.1mol/L NaClO��Һ��pH��0.1mol/L Na2SO3��Һ��pH���������ˮ��̶�Խ������Һ�и��������Ũ��ԽС����������Ũ�ȴ�С˳����c��SO32-����c��CO32-����c��HCO3-����c��HSO3-����
�ʴ�Ϊ�����ڣ�c��SO32-����c��CO32-����c��HCO3-����c��HSO3-����
���� ���⿼����ԭ����Ϊ��Ƶ���㣬�漰��⡢����Ũ�ȴ�С�Ƚϡ�������ԭ��Ӧ�����淴Ӧ��֪ʶ�㣬��ȷ��ѧ��Ӧԭ�������������ǽⱾ��ؼ���֪������ƽ�ⳣ����С���������ǿ�����������ˮ��̶���Դ�С��ϵ����Ŀ�ѶȲ���

 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д�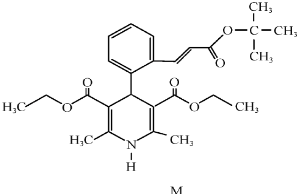
���й���M��˵����ȷ���ǣ�������
| A�� | ���ڷ����廯���� | B�� | ��FeCl3��Һ����ɫ | ||
| C�� | ����ʹ���Ը��������Һ��ɫ | D�� | 1molM��ȫˮ������2mol�� |
| A�� | HCl | B�� | CO2 | C�� | NH3 | D�� | CO |
| A�� | ��ϡ��ˮ��ͨ�����CO2��NH3•H2O+CO2�TNH4++HCO3- | |
| B�� | ��NH4��2SO4��Һ�м�������Ba��OH��2��Ba2++SO42-=BaSO4�� | |
| C�� | ��ϡHNO3�ܽ�FeS���壺FeS+2H+�TFe2++H2S�� | |
| D�� | ����������Һ������ʵ�����ϡ�����ϣ�Ca2++OH-+H++SO42-�TCaSO4��+H2O |
| A�� | �뾶��Y2-��Z-��X+��W3+ | B�� | ��ԭ�ԣ�Y2-��Z- | ||
| C�� | �����ԣ�W3+��X+ | D�� | ��������c��d��b��a |
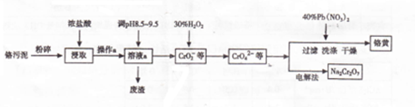
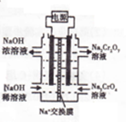
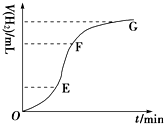 �����ô�����п����ϡ���ᷴӦ��ȡH2����ش�
�����ô�����п����ϡ���ᷴӦ��ȡH2����ش�