题目内容
8.广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种功能的装置.如图图中各装置可用作测量气体体积的是( )| A. |  | B. | 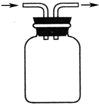 | C. |  | D. | 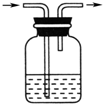 |
分析 A.该装置是排液量气装置;
B.该装置可作为安全瓶;
C.该装置混气装置;
D.该装置是洗气装置.
解答 解:A.该装置是排液量气装置,故A正确;
B.该装置可作为安全瓶防倒吸,因为进气管较短(刚漏出瓶塞)若发生倒吸,倒吸液会被盛装在B 瓶中,不会再倒流到前一装置,从而防止倒吸,故B错误;
C.该装置是混气装置,进入C 瓶中两气体在C 瓶中充分混合,故C错误;
D.该装置是洗气装置,故D错误.
故选A.
点评 本题考查气体收集装置、防倒吸安全瓶,题目难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
18.与下列实验事实所对应的相应结论正确的是
( )
| 实验事实 | 结论 | |
| ① | HCl的水溶液中存在H+和Cl- | HCl是离子化合物 |
| ② | NO2通入水中,发生反应,产物中有HNO3 | NO2是酸性氧化物 |
| ③ | 向FeCl3溶液中加入铜片,溶液逐渐变为蓝色 | 氧化性:Fe3+>Cu2+ |
| ④ | 等物质的量的Na和Al都完全反应,Al失电子多 | 金属性:Al>Na |
| ⑤ | 某无色溶液中加入氢氧化钠浓溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定有NH4+ |
| A. | ①② | B. | ①②④ | C. | ③⑤ | D. | ③④⑤ |
3.某同学组装了如图所示的电化学装置,则下列说法正确的是( )


| A. | 图中甲池为原电池装置,Cu电极发生还原反应 | |
| B. | 实验过程中,甲池左侧烧杯中NO3-的浓度不变 | |
| C. | 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是足量AgNO3溶液 | |
| D. | 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量不变 |
13.如图是实验室模拟煤的干馏的实验装置,下列叙述错误的是( )


| A. | 上图实验中发生了化学变化 | |
| B. | 液体Y是一种纯净物 | |
| C. | 气体Z易燃,可还原CuO | |
| D. | 水溶液X的pH>7,液体Y是黑色黏稠状的煤焦油 |
20.下列物质转化在给定条件下不能实现的是( )
| A. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$Fe(OH)3(胶体) | |
| B. | Al2O3$→_{△}^{NaOH(aq)}$NaAlO2(aq)$\stackrel{HCl(aq)}{→}$AlCl3 | |
| C. | FeS2$\frac{\underline{\;燃烧\;}}{\;}$SO3$\frac{\underline{\;H_{2}O\;}}{\;}$H2SO3 | |
| D. | 饱和NaCl(aq)$\frac{\underline{\;NH_{3}CO_{3}\;}}{\;}$NaHCO3$\stackrel{△}{→}$Na2CO3 |
16.煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如下表:
试回答下列问题:
(1)上述逆向反应是:放热 反应(选填:放热、吸热)
(2)在800℃发生反应,以表中的量投入恒容反应器,其中向正反应方向移动的有CDE.
(3)已知在一定温度下:
C(s)+CO2(g)?(g)平衡常数K;
C(s)+H2O(g)?(g)+H2(g)平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g) 平衡常数K2,则K、K1、K2之间的关系是:K=$\frac{K{\;}_{1}}{K{\;}_{2}}$.
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为75%.
(5)若在800℃进行,起始时CO和H2O(g)均为1mol,一段时间后反应达平衡,保持温度不变,继续向平衡体系中通入1molH2O(g),重新平衡时CO转化率为66.7%.
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K=$\frac{4}{9}$.
已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数Kc | 9.94 | 9 | 1 |
(1)上述逆向反应是:放热 反应(选填:放热、吸热)
(2)在800℃发生反应,以表中的量投入恒容反应器,其中向正反应方向移动的有CDE.
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 0.5 | 3 | 2 | 3 |
| n(H2O) | 5 | 2 | 3 | 2 | 1 |
C(s)+CO2(g)?(g)平衡常数K;
C(s)+H2O(g)?(g)+H2(g)平衡常数K1;
CO(g)+H2O(g)?H2(g)+CO2(g) 平衡常数K2,则K、K1、K2之间的关系是:K=$\frac{K{\;}_{1}}{K{\;}_{2}}$.
(4)若在500℃时进行,若CO、H2O的起始浓度均为0.020mol/L,在该条件下,CO的最大转化率为75%.
(5)若在800℃进行,起始时CO和H2O(g)均为1mol,一段时间后反应达平衡,保持温度不变,继续向平衡体系中通入1molH2O(g),重新平衡时CO转化率为66.7%.
(6)在VL密闭容器中通入10molCO和10mol水蒸气,在T℃达到平衡,然后急速除去水蒸气(除水蒸气时各物质的物质的量不变),将混合气体燃烧,测得放出的热量为2842kJ(已知CO燃热为283kJ/mol,H2燃烧热为286kJ/mol),则T℃平衡常数K=$\frac{4}{9}$.
