题目内容
9.A是石油裂解的主要产物之一.标准状况下,A对氢气的相对密度是14,乳酸是一种常见的有机酸,用途广泛.高吸水性树脂F是一种高分子材料,可用于干旱地区抗旱保水、改良土壤、改造沙漠,还可制作尿不湿.下图是以A为原料制取高吸水性树脂F的合成路线图:
已知:
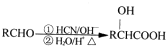
请回答下列问题:
(1)A的结构简式是CH2=CH2,A→B的→类型是加成反应;
(2)B→C的化学方程式是CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)乳酸有多种同分异构体,其中只含醛基和烃基两种官能团(不包括一个碳原子上连有两个烃基,不考虑立体异构)的同分异构体的结构简式为CH2OHCHOHCHO;
(4)一定条件下,两分子乳酸反应生成一种六元环状化合物,此反应的化学方程式是
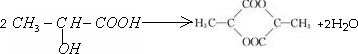 ;
;(5)由E到F反应的化学方程式是nCH2=CHCOONa$\stackrel{一定条件下}{→}$
 .
.
分析 A对氢气的相对密度是14,则A的相对分子质量是28,为CH2=CH2;根据题给信息知,C中含有醛基,则C为CH3CHO,B发生氧化反应生成乙醛,B为CH3CH2OH,A发生加成反应生成B,乳酸结构简式为 ;
;
D能和NaOH反应说明D中还含有羧基,则乳酸发生消去反应生成D,D结构简式为CH2=CHCOOH,E结构简式为CH2=CHCOONa,E发生加聚反应生成F,F结构简式为 ,据此分析解答.
,据此分析解答.
解答 解:A对氢气的相对密度是14,则A的相对分子质量是28,为CH2=CH2;根据题给信息知,C中含有醛基,则C为CH3CHO,B发生氧化反应生成乙醛,B为CH3CH2OH,A发生加成反应生成B,乳酸结构简式为 ;
;
D能和NaOH反应说明D中还含有羧基,则乳酸发生消去反应生成D,D结构简式为CH2=CHCOOH,E结构简式为CH2=CHCOONa,E发生加聚反应生成F,F结构简式为 ,
,
(1)A是乙烯,A的结构简式是CH2=CH2,A加成反应生成B,A→B的→类型是加成反应,
故答案为:CH2=CH2;加成反应;
(2)B→C乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(3)乳酸有多种同分异构体,其中只含醛基和烃基两种官能团(不包括一个碳原子上连有两个烃基,不考虑立体异构)的同分异构体的结构简式为CH2OHCHOHCHO,故答案为:CH2OHCHOHCHO;
(4)一定条件下,两分子乳酸反应生成一种六元环状化合物,此反应的化学方程式是 ,
,
故答案为: ;
;
(5)E结构简式为CH2=CHCOONa,E发生加聚反应生成F,F结构简式为 ,由E到F反应的化学方程式是nCH2=CHCOONa$\stackrel{一定条件下}{→}$
,由E到F反应的化学方程式是nCH2=CHCOONa$\stackrel{一定条件下}{→}$ ,
,
故答案为:nCH2=CHCOONa$\stackrel{一定条件下}{→}$ .
.
点评 本题考查有机物推断,侧重考查学生分析判断能力,根据反应条件及官能团的性质进行推断,注意结构题给信息,知道断键和成键方式,题目难度不大.

| A. | 放入敞口的容器中 | |
| B. | 放入浸泡过高锰酸钾溶液硅土的密封容器中 | |
| C. | 放入密封的容器中 | |
| D. | 放入充有少量乙烯的密封容器中 |
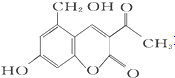 M(假蜜环菌素)
M(假蜜环菌素)| A. | M的分子式为C12H10O5 | |
| B. | 1 mol M最多可和6mol H2发生加成反应 | |
| C. | M可发生水解反应 | |
| D. | M可与 HBr反应 |
| 操作 | 实验现象 | 结论 | |
| A | 向NaBr溶液中加入氯水,再加入淀粉KI溶液 | 溶液变蓝 | 氧化性:Cl2>Br2>I2 |
| B | 将铝片放入盐酸中 | 产生气泡的速率开始较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 得到蓝色溶液 | 蔗糖水解产物没有还原性 |
| D | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 铜矿石在细菌作用下直接转换为单质铜,这个过程中叫做生物炼铜 | |
| B. | 人们通常用标准燃烧热或热值来衡量燃料燃烧放出热量的大小,相同条件下,某物质的热值越高,其标准燃烧越大 | |
| C. | 铅蓄电池是最常见的二次电池,可根据硫酸的密度来判断铅蓄电池是否需要充电 | |
| D. | “地沟油”禁止食用,但可以通过物理变化制肥皂 |
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | SF6中的空间构型为正四面体形 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |

| A. | 等体积的三种酸与足量Mg反应,HX放出气体的体积最小 | |
| B. | 三种酸等体积混合后与NaOH溶液反应,当HX恰好完全反应时:c(Y-)>c(X-)>c(OH-)>c(H+) | |
| C. | 根据曲线,可得0.1mol•L-1HX溶液中由水电离出的c(H+)为10-4mol•L-1 | |
| D. | 将HY与HZ的稀溶液混合后所得溶液中:c(H+)=$\frac{{K}_{a}(HY)•c(HY)}{c({H}^{+})}$+c(Z-)+c(OH-) |
| A. | 电解精炼铜时,负极反应式:Cu2++2e-=Cu | |
| B. | 氯碱工业和电解精炼铜中,阳极都是氯离子放电放出氯气 | |
| C. | 在氯碱工业中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 | |
| D. | 电解精炼铜时,应用粗铜作阳极、精铜作阴极,可溶性铜盐作电解质溶液 |
| A. | NH3和Cl2 | B. | NH3和HBr | C. | SO2和O2 | D. | SO2和H2S |