题目内容
下列离子方程式正确的是
| A.等物质的量的Ba(OH)2与明矾[KAl(SO4)2·12H2O]加入足量水中: 3Ba2++6OH-+2Al3++3SO  ===3BaSO4↓+2Al(OH)3↓ ===3BaSO4↓+2Al(OH)3↓ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O |
C.H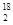 O中投入Na2O2固体:2H O中投入Na2O2固体:2H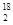 O+2Na2O2===4OH-+4Na++18O2↑ O+2Na2O2===4OH-+4Na++18O2↑ |
| D.CuCl2溶液中加入H2S溶液:Cu2++S2-===CuS↓ |
A
解析试题分析:B选项三价的铁离子就有氧化性,溶液中不可能存在碘离子,碘离子被氧化为碘单质。因此B选项是错误的。C选项氧气中的氧主要来自于过氧化钠中的氧,所以C选项下是错误的。D选项硫化氢属于弱电解质,不能写成离子形式,因此D选项是错误的。
考点:考查离子反应方程式书写的相关知识点

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是 (. )
| 选项 | 离子或分子 | 要求 |
| A | K+ 、NO3-、Cl-、HS- | c(K+)<c(Cl-) |
| B | Fe3+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、CH3COOH | 滴加NaOH溶液立即有气体产生 |
| D | Na+、HCO3-、Mg2+、SO42- | 逐滴滴加氨水立即有沉淀产生 |
下列叙述中,能证明某物质是强电解质或弱电解质的是
| A.某物质熔化时不导电,则该物质为弱电解质 |
| B.某物质不是离子化合物,而是极性共价化合物,则该物质为弱电解质 |
| C.某一元酸2 mol与足量Zn完全反应生成1 molH2,则该酸为强酸 |
| D.溶液中已电离的离子和未电离的分子共存,则该物质为弱电解质 |
水溶液中能大量共存的一组离子是
| A.Na+、Ca2+、Cl-、SO42- | B.Fe2+、H+ 、SO32-、ClO- |
| C.Mg2+、NH4+、Cl-、SO42- | D.K+、Fe3+、NO3-、SCN- |
能正确表示下列反应的离子方程式是
| A.NaHCO3的水解:HCO3-+H2O=CO32-+H3O+ |
| B.用银氨溶液检验乙醛的醛基: CH3CHO+2Ag(NH3)2OH  CH3COO-+NH4++3NH3+2Ag↓+H2O CH3COO-+NH4++3NH3+2Ag↓+H2O |
C.向苯酚钠溶液中通入少量的CO2:CO2+H2O+2C6H5O- 2C6H5OH+2CO32- 2C6H5OH+2CO32- |
| D.泡沫灭火剂的原理:Al3++3HCO3-=Al(OH)3↓+3CO2↑ |
 的性质___________(填序号,下同)。
的性质___________(填序号,下同)。 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________ B.
B.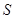 C.
C. D.
D.
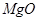 、
、 、
、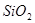 、
、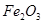 组成。其中
组成。其中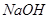 溶液至过量、过滤,滤渣中的主要成分是_________。
溶液至过量、过滤,滤渣中的主要成分是_________。