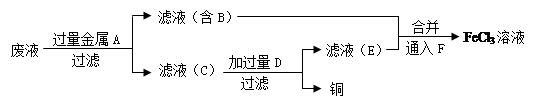
题目内容
(18分)⑴有下列物质:①铜 ②硫酸钡固体 ③氨水 ④氢氧化钠固体 ⑤熔融硝酸钾;⑥乙醇; ⑦稀硫酸; ⑧金刚石; ⑨二氧化硫 ; ⑩冰醋酸。
其中能导电的有 ;属于非电解质的有 ;属于强电解质的有 ;(填序号)
⑵常温下,将pH=3的盐酸和pH=11的氨水等体积混合后溶液呈 性,溶液中c(NH4+)与c(Cl-)的大小关系是:c(NH4+) c(Cl-);
⑶常温下,0.010mol·L-1盐酸和0.010mol·L-1氨水的pH之和 14,常温下,pH=2的盐酸和pH=12的氨水,分别加水稀释10倍后,两溶液的pH之和 14(填>,<或=)
⑷用物质的量浓度为0.04 mol·L-1的盐酸恰好中和OH-浓度为1.0×10-3 mol·L-1的氨水溶液20mL,消耗盐酸12.5mL,则此氨水物质的量浓度为 mol·L-1;电离度为 。
⑴ ①③⑤⑦ ;⑥⑨ ;②④⑤ ;⑵ 碱性;> ;⑶ <;> ;⑷ 0.025 ; 4% 。
解析试题分析:⑴①铜是金属单质,能导电;②硫酸钡固体是盐,属于电解质。熔融状态下能完全电离,是强电解质; ③氨水是混合物,能导电; ④氢氧化钠固体是电解质,由于是固体,所以不能导电;在水中或熔融状态下能完全电离,是强电解质; ⑤熔融硝酸钾是电解质,因为在熔融态,因此可以导电;在水中或熔融状态下能完全电离,是强电解质;⑥乙醇是非电解质,不能导电; ⑦稀硫酸是混合物,能导电; ⑧金刚石是非金属单质,不能导电; ⑨二氧化硫是非电解质,不能导电; ⑩冰醋酸是电解质,由于都是以电解质分子的形式存在,所以不能导电。在水溶液中存在电离平衡,因此是弱电解质。因此其中能导电的有①③⑤⑦;属于非电解质的有⑥⑨;属于强电解质的有②④⑤ ;⑵常温下,Kw=10-14.将pH=3的盐酸,c(H+)=10-3mol/L;pH=11的氨水c(OH-)=10-3mol/L.由于一水合氨是弱电解质,所以c(NH3·H2O)> 10-3mol/L.当二者等体积混合时,由于碱过量所以混合后溶液呈碱性。在溶液中存在电荷守恒c(Cl-)+ c(OH-)= c(H+)+c(NH4+).又由于在混合溶液中c(OH-)> c(H+),所以c(Cl-)< c(NH4+)。⑶常温下,Kw=10-14.0.010mol·L-1盐酸c(H+)=10-2mol/L,pH=2; 0.010mol·L-1氨水c(OH-)< 10-2mol/L.pH<12.因此二者的pH之和小于14。在常温下,pH=2的盐酸加水稀释10倍后pH=3;而由于一水合氨是弱电解质,所以 pH=12的氨水加水稀释10倍后,未电离的电解质分子会继续电离,使氢氧根离子的浓度又略有增大,所以pH>11.因此两溶液的pH之和>14。(4)一元酸碱混合恰好完全反应时,二者的物质的量相等。C(氨水)="(0.04" mol/L×0.0125L)÷0.02L=0.025mol/L. 因为c(OH-)=1.0×10-3 mol/L,所以其电离度为:(1.0×10-3 mol/L÷0.025mol/L)×100%=4%。
考点:考查电解质、非电解质、强电解质、弱电解质的概念、酸碱混合溶液中离子的浓度、溶液的pH弱电解质电离度的计算的知识。

 阅读快车系列答案
阅读快车系列答案下列物质属于纯净物的是
| A.钢 | B.液氯 | C.空气 | D.氨水 |
I .用序号回答下列各题:
① 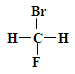 和
和 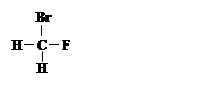
②1H—、2H、3H +、D2 ③淀粉和纤维素
④ 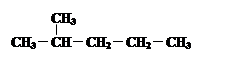 和
和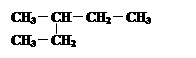
⑤16O2、18O3 ⑥235U、238U
其中互为同位素的是 。
互为同素异形体的是 。
互为同分异构体的是 。
是同一种化合物的是 。
II. 请选择合适的试剂检验某物质中是否含括号内物质:
| 序号 | 原物质(需检验物质) | 试剂 |
| ① | CO2(SO2) | |
| ② | 乙醇(水) | |
| ③ | 直馏汽油( 裂化汽油) | |
Ⅲ.某元素R气态氢化物化学式为HnR。若最高价氧化物对应水化物分子中有b个氧原子,则其最高价氧化物对应水化物化学式通常表达为 。(含n和b)
化工生产中常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是________(填物质名称)。
(2)“三酸”与“两碱”之间的反应,若用化学方程式表示有六个(酸过量时) ,若用离子方程式表示却只有两个,请写出这两个离子方程式:(酸过量时)_____________________________、______________________。
(3)“三酸”常用于溶解金属和金属氧化物。下列块状金属在常温时能全部溶于足量浓硝酸的是________。
| A.Au | B.Cu |
| C.Al | D.Fe |
①________,②Na2CO3,③________,④NaHCO3。
下列离子方程式正确的是
| A.等物质的量的Ba(OH)2与明矾[KAl(SO4)2·12H2O]加入足量水中: 3Ba2++6OH-+2Al3++3SO  ===3BaSO4↓+2Al(OH)3↓ ===3BaSO4↓+2Al(OH)3↓ |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+===Fe3++3H2O |
C.H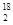 O中投入Na2O2固体:2H O中投入Na2O2固体:2H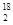 O+2Na2O2===4OH-+4Na++18O2↑ O+2Na2O2===4OH-+4Na++18O2↑ |
| D.CuCl2溶液中加入H2S溶液:Cu2++S2-===CuS↓ |