题目内容
17.下列化学反应的离子方程式书写正确的是( )| A. | 用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O | |
| B. | Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+OH-═CO32-+H2O | |
| C. | 利用腐蚀法制作印刷线路板:Fe3++Cu═Fe2++Cu2+ | |
| D. | 钠与水反应:Na+H2O═Na++OH-+H2↑ |
分析 A.二者反应生成二氧化碳和水;
B.氢氧化钠过量反应生成碳酸钠和碳酸钙、水;
C.电荷不守恒;
D.原子个数不守恒;
解答 解:A.用小苏打治疗胃酸过多,离子方程式:HCO3-+H+═CO2↑+H2O,故A正确;
B.Ca(HCO3)2溶液与过量NaOH溶液反应,离子方程式:Ca2++2HCO3-+2OH-═CO32-+2H2O+CaCO3↓,故B错误;
C.利用腐蚀法制作印刷线路板,离子方程式:2Fe3++Cu═2Fe2++Cu2+,故C错误;
D.钠与水反应,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故D错误;
故选:A.
点评 本题考查了离子方程式书写正误判断,明确离子方程式书写方法是解题关键,注意离子反应遵循客观事实、遵循原子个数、电荷数守恒规律.

练习册系列答案
相关题目
7.“细节决定成败”化学实验中尤其要注重细节.下列实验操作或设计正确的是( )
| A. | 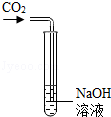 检验生成的气体是CO2 | B. | 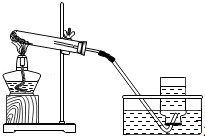 加高锰酸钾制氧气 | ||
| C. | 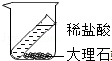 验证质量守恒定律 | D. | 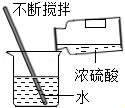 实验室稀释浓硫酸 |
5.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 一个水分子的质量为18NA g | |
| B. | 常温常压下,22.4L氯气与足量金属钠充分反应,转移的电子数为2 NA | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 通常状况下,32g 混合气体(O2和O3 )所含的氧原子数一定为2NA |
12.有Fe2+﹑NO3-﹑Fe3+、NH4+﹑H2O 和H+六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述错误的是( )
| A. | 氧化剂与还原剂的物质的量之比为8:1 | |
| B. | 还原产物为NH4+ | |
| C. | 若有1molNO3-参加还原反应,则转移3mol e- | |
| D. | 若把该反应设计为原电池,则负极反应为 Fe2+-e _=Fe3+ |
9.三氯化氮分子中每个原子的最外层均达到8电子稳定结构,且氮与氯的共用电子对偏向氮原子.则下列关于三氯化氮的叙述正确的是( )
| A. | NCl3为非极性分子 | |
| B. | NCl3跟水反应的产物为NH3和HClO | |
| C. | NCl3跟水反应生成NH4Cl、O2和Cl2 | |
| D. | 在NCl3分子中N为+3价,跟水发生水解反应的产物是HNO2和HCl |
6.“关爱生命,拥抱健康”.人们在日常生活中的下列行为会损害人体健康的是( )
| A. | 用碳酸氢钠焙制糕点 | B. | 在易碎的食品包装袋中充入氮气 | ||
| C. | 炖排骨时滴加一定量的食醋 | D. | 用霉变花生(含黄曲霉素)压榨花生油 |
7.下列有关化学用语和概念的表达理解正确的是( )
| A. | 立体烷 和苯乙烯 和苯乙烯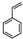 互为同分异构体 互为同分异构体 | |
| B. | 1,3-丁二烯的键线式可表示为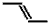 | |
| C. | 二氟化氧分子电子式为  | |
| D. | H216O、D216O、H218O、D218O互为同素异形体 |
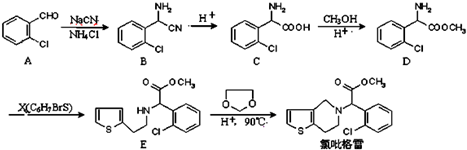
 .
. .
.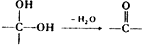 ,
,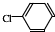 中氯原子较难水解物质A(
中氯原子较难水解物质A(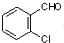 ),可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式
),可由2-氯甲苯为原料制得,写出以两步制备A的化学方程式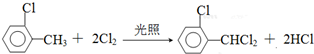 、
、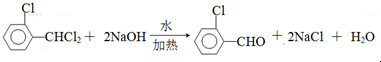 .该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式
.该合成的第一步主要存在产率低的问题,请写出该步可能存在的有机物杂质的结构简式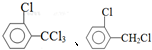 .
.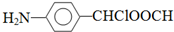 .
.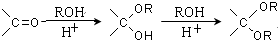 写出由乙烯、甲醇为有机原料制备化合物
写出由乙烯、甲醇为有机原料制备化合物 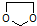 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: