题目内容
7.根据下面的合成路线及所给信息填空:
(1)A的结构简式是
 ,名称是环己烷
,名称是环己烷(2)①的反应类型是取代反应、③的反应类型是加成反应
(3)反应④的化学方程式是

(4)下列有关有机物
 具有的性质叙述正确的是C、D
具有的性质叙述正确的是C、DA.不能使酸性高锰酸钾溶液褪色
B.易溶于水
C.1mol该有机物最多与1molH2发生加成反应
D.能使溴水褪色.
分析 由合成路线可知,反应①为光照条件下的取代反应,所以A为 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为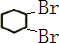 ,反应④为卤代烃的消去反应,生成环己二烯,结合对应物质的结构和性质以及题目要求解答该题.
,反应④为卤代烃的消去反应,生成环己二烯,结合对应物质的结构和性质以及题目要求解答该题.
解答 解:由合成路线可知,反应①为光照条件下的取代反应,所以A为 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为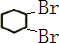 ,反应④为卤代烃的消去反应,生成环己二烯,
,反应④为卤代烃的消去反应,生成环己二烯,
(1)由以上分析可知A为 ,名称为环己烷,故答案为:
,名称为环己烷,故答案为: ;环己烷;
;环己烷;
(2)反应①为取代反应,③为加成反应,故答案为:取代反应;加成反应;
(3)反应④为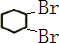 的消去反应,反应的化学方程式为
的消去反应,反应的化学方程式为 ,
,
故答案为: ;
;
(4)在 有一个碳碳双键,所以能使酸性高锰酸钾溶液褪色,1mol
有一个碳碳双键,所以能使酸性高锰酸钾溶液褪色,1mol 最多与1molH2发生加成反应,能使溴水褪色,
最多与1molH2发生加成反应,能使溴水褪色, 难溶于水,
难溶于水,
故选C、D.
点评 本题考查有机物的合成与推断,为高考常见题型,明确反应条件与反应类型的关系来推出各物质是解答本题的关键,注意卤代烃的水解、消去反应的条件,题目难度不大.

练习册系列答案
相关题目
17.现有三种物质A、B、C,其中有一种是酸,一种是碱,一种是盐,溶于水后电离,可以产生下表中的离子:
为鉴别它们,分别完成以下实验,其结果如下:
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出物质B、C的化学式:BH2SO4 CBa(OH)2
(2)写出下列反应的离子方程式:
①A溶液与C溶液反应:Ba2++CO32-=BaCO3↓;
②B溶液与碳酸氢钠溶液反应:H++HCO3-=H2O+CO2↑.
③将少量的C溶液滴入足量的碳酸氢钾溶液反应:Ba2++2OH-+2HCO3-=2H2O+CO32-+BaCO3↓.
| 阳离子 | Na+ H+ Ba2+ |
| 阴离子 | OH- CO${\;}_{3}^{2-}$ SO${\;}_{4}^{2-}$ |
①A溶液与B溶液反应生成无色气体X,气体X可以和C溶液反应生成沉淀E,沉淀E可与B溶液反应;
②B溶液与C溶液反应生成白色沉淀D,沉淀D不溶于稀硝酸.
请根据上述实验结果,填空:
(1)写出物质B、C的化学式:BH2SO4 CBa(OH)2
(2)写出下列反应的离子方程式:
①A溶液与C溶液反应:Ba2++CO32-=BaCO3↓;
②B溶液与碳酸氢钠溶液反应:H++HCO3-=H2O+CO2↑.
③将少量的C溶液滴入足量的碳酸氢钾溶液反应:Ba2++2OH-+2HCO3-=2H2O+CO32-+BaCO3↓.
15.下列电离方程式错误的是( )
| A. | CaCl2═Ca2++2Cl- | B. | NaHSO4═Na++H++SO42- | ||
| C. | HNO3═H++NO3- | D. | NaHCO3═Na++H++CO32- |
12. 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol.N2的平衡转化率(α)与体系总压强(P)的关系如图所示.下列说法正确的是( )| A. | 将1.0 mol氮气、3.0 mol氢气,置于1 L密闭容器中发生反应,放出的热量为 92.4 kJ | |
| B. | 平衡状态由A变到B时,平衡常数K (A)<K (B) | |
| C. | 上述反应在达到平衡后,增大压强,H2的转化率提高 | |
| D. | 升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速度减小 |
19.下列有关混合物的分离与提纯的说法正确的是( )
| A. | 由于碘在乙醇中的溶解度较大,所以可用乙醇把碘水中的碘萃取出来 | |
| B. | 水的沸点为100℃,乙醇的沸点为78.5℃,所以用加热蒸馏的方法使含水乙醇变为无水乙醇 | |
| C. | 由于汽油和水不互溶,因此可用分液的方法将二者分离 | |
| D. | NaCl溶液度随温度下降而减小,所以用冷却法从热的含少量KNO3的NaCl浓溶液中分离得到纯净的NaCl |
1.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 1 mol聚乙烯含有的原子数目为6NA | |
| B. | 标况下1 L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA/22.4 | |
| C. | 1 mol甲基含7 NA个电子 | |
| D. | 2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
2.现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.请根据下列相关信息,回答问题.
(1)A基态原子中能量最高的电子,其电子云在空间有3个方向,原子轨道呈纺锤形.
(2)某同学根据上述信息,所画的B电子排布图如图 ,违背了泡利原理.
,违背了泡利原理.
(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(2)某同学根据上述信息,所画的B电子排布图如图
 ,违背了泡利原理.
,违背了泡利原理.(3)F位于周期表中第四周期、ⅦB族、d区,其基态原子有25种运动状态.
(4)CD3中心原子的杂化方式为sp3,用价层电子对互斥理论推测其分子空间构型为三角锥形,检验E元素的方法是焰色反应.