题目内容
2.下列有关化学用语使用正确的是( )| A. | NH4Br的电子式: | |
| B. | S2-的结构示意图: | |
| C. | 比例模型  可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 | |
| D. | 丙烷的结构简式为:CH3CHCH3 |
分析 A.溴化铵为离子晶体,由铵根离子与溴离子通过离子键结合在一起,溴离子最外层电子未标注;
B.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,用小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数;
C.比例模型既能表示分子的空间结构,又能表示出分子中各原子的相对大小,与分子的真实结构最接近;
D.丙烷为烷烃,碳原子都是饱和碳原子,写出四个共价键.
解答 解:A.溴化铵是离子化合物,由铵根离子与溴离子构成,电子式为: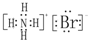 ,故A错误;
,故A错误;
B.S2-的质子数为16,核外电子数为18,各层电子数分别为2、8、8,硫离子结构示意图为 ,故B正确;
,故B正确;
C.甲烷结构和四氯化碳结构不同,氯原子比碳原子大,比例模型中原子比例大小不同,故C错误;
D.丙烷的结构简式为:CH3CH2CH3,故D错误;
故选B.
点评 本题考查化学用语的分析判断,掌握基础和书写规范,理解含义是解题关键,题目难度不大.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
12.金刚石和石墨是碳元素的两种结构不同的单质(同素异形体).在100KPa时,1mol石墨转化为金刚石,要吸收1.895kJ的热量.据此试判断下列结论正确的是( )
| A. | 金刚石比石墨稳定 | B. | 石墨和金刚石是碳元素的同位素 | ||
| C. | 1mol石墨比1mol金刚石的总能量高 | D. | 金刚石转化为石墨属于化学变化 |
13.下列关于有机物的说法正确的是( )
| A. | 纯净物C4H8的核磁共振氢谱峰最多为4 | |
| B. | 化学式为C8H8的有机物,一定能使酸性高锰酸钾溶液褪色 | |
| C. |  的同分异构体中,可以有醇类、但没有酚类物质 的同分异构体中,可以有醇类、但没有酚类物质 | |
| D. | 1 mol 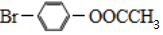 最多能与2 mol NaOH反应 最多能与2 mol NaOH反应 |
10.短周期主族元素X、Y、Z、W原子序数依次增大,X的原子失去一个电子后即为质子,X、Z同主族,Y的原子L层有5个电子,W的单质常温下呈气态.下列说法正确的是( )
| A. | 原子半径:r(X)<r(Y)<r(Z)<r(W) | |
| B. | Y的最高价氧化物的水化物酸性比W的强 | |
| C. | Z的一种氧化物可能既含离子键又含共价键 | |
| D. | X、Y、W三种元素一定只能组成共价化合物 |
17.化学与生活息息相关,下列说法不正确的是( )
| A. | 用食醋可除去热水壶内壁的水垢 | |
| B. | 工业上电解熔融状态的Al2O3制备Al | |
| C. | 油脂和蛋白质都是高分子化合物 | |
| D. | 利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程 |
7.根据下列有关实验得出的结论一定正确的是
| 选项 | 操作 | 现象与结论 |
| A | 同温时,等质量的锌粒分别与加有胆矾和未加胆矾的足量的稀硫酸反应 | 产生氢气量两者相等 |
| B | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液 | 溶液变黄,氧化性:H2O2>Fe3+ |
| C | 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应 | 粉状大理石产生气泡更快,反应速率:粉状大理石>块状大理石 |
| D | 向浓度均为0.1 mol•L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀,Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
14.下列各组原子序数所表示的两种元素,能形成AB2型离子化合物的是( )
| A. | 1和7 | B. | 6和8 | C. | 11和16 | D. | 12和17 |
11. 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )
 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述不正确的是( )| A. | Zn电极上发生氧化反应 | |
| B. | 电池工作后,甲池的SO42-微粒数减少 | |
| C. | 电池工作后,甲池溶液的阳离子移动到乙池 | |
| D. | 电池工作后,乙池中的Cu电极质量增加 |
 与
与 F.
F.  与
与