题目内容
在0.1mol?L-1的NaHCO3溶液中,下列关系式正确的是( )
| A、c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-) |
| B、c(Na+)>c(CO32->c(HCO3-)>c(OH-) |
| C、c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2 c(CO32-) |
| D、c(HCO3-)+c(CO32-)=0.1 mol?L-1 |
考点:离子浓度大小的比较
专题:
分析:A、碳酸氢钠溶液中遵循物料守恒,根据物料守恒进行判断;
B、NaHCO3溶液呈碱性,HCO3-的水解程度大于电离程度,且水解程度很小;
C、溶液中存在电荷守恒,根据碳酸氢钠溶液中的电荷守恒进行判断;
D、C在溶液中以HCO3-、CO32-、H2CO3形式存在.
B、NaHCO3溶液呈碱性,HCO3-的水解程度大于电离程度,且水解程度很小;
C、溶液中存在电荷守恒,根据碳酸氢钠溶液中的电荷守恒进行判断;
D、C在溶液中以HCO3-、CO32-、H2CO3形式存在.
解答:
解:A、根据元素守恒n(Na)=n(C),C在溶液中以HCO3-、CO32-、H2CO3形式存在,则c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故A正确;
B、NaHCO3溶液呈碱性,HCO3-的水解程度大于电离程度,且水解程度很小,溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-),故B错误;
C、碳酸氢钠溶液一定存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D、C在溶液中以HCO3-、CO32-、H2CO3形式存在,c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol?L-1,故D错误;
故选AC.
B、NaHCO3溶液呈碱性,HCO3-的水解程度大于电离程度,且水解程度很小,溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-),故B错误;
C、碳酸氢钠溶液一定存在电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D、C在溶液中以HCO3-、CO32-、H2CO3形式存在,c(HCO3-)+c(CO32-)+c(H2CO3)=0.1 mol?L-1,故D错误;
故选AC.
点评:本题考查离子浓度的大小比较,题目难度中等,注意把握弱电解质的电离和盐类水解的原理,从守恒的角度比较离子浓度大小是常用的方法.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案
相关题目
西维因是一种高效低毒杀虫剂,在碱性条件下可水解:则下列说法正确的是( )
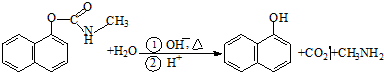

| A、西维因是一种芳香烃 |
| B、西维因分子中所有碳原子一定共面 |
| C、可用FeCl3溶液检验西维因是否发生水解 |
| D、在Ni催化下1mol西维因最多能与6molH2加成 |
中学常见物质A、B、C、D、E、X,存在图转化关系(部分生成物和反应条件略去).下列推断不正确的是( )A
B
C
D.
| E |
| E |
| X |
| A、若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C |
| B、若D是一种强碱,则A、B、C均可与X反应生成D |
| C、若D为NaCl,且A可与C反应生成B,则E可能是CO2 |
| D、若D是一种白色沉淀,在空气中最终变为红褐色,则A可能是铁 |
 如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C处分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等,下列说法正确的是( )
如图所示,在一个容积固定的恒温容器中,有两个可左右滑动的密封隔板,在A、B、C处分别充入等质量的X、H2、Y三种气体,当隔板静止时,A、C内的气体密度相等,下列说法正确的是( )| A、X的相对分子质量等于Y的相对分子质量 |
| B、X的相对分子质量比Y的相对分子质量小 |
| C、气体的体积:V(X)>V(H2)>V(Y) |
| D、物质的量:n(X)<n(H2)<n(Y) |
 反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温D23mtt1C23mt度,y轴表示平衡混合气体中G的体积分数.据此可判断( )
反应:L(s)+aG(g)?bR(g)达到平衡,温度和压强对该反应的影响如图所示,图中:压强p1>p2,x轴表示温D23mtt1C23mt度,y轴表示平衡混合气体中G的体积分数.据此可判断( )| A、上述反应是吸热反应 |
| B、上述反应是放热反应 |
| C、a>b |
| D、无法确定a、b的大小 |

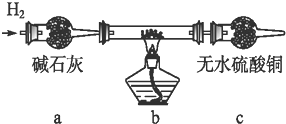 实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.
实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.