题目内容
下列各表述与示意图一致的是( )


| A、图①表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 KOH溶液,溶液的pH随加入酸体积的变化 |
| B、图②中曲线表示反应N2(g)+3H2(g)═2NH3(g)△H<0 正、逆反应的平衡常数K随温度的变化 |
| C、图③表示醋酸溶液滴定NaOH和氨水混合溶液的电导率曲线 |
| D、图④中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
考点:酸碱混合时的定性判断及有关ph的计算,反应热和焓变,化学平衡常数的含义,电解质溶液的导电性
专题:图示题,基本概念与基本理论
分析:A、在滴入20mL氯化氢时,氢氧化钠就与氯化氢恰好反应,滴定曲线应该有一个滴定突变;
B、该反应为放热反应,温度升高,平衡向着逆向移动,K逆中增大,而K正减小;
C、醋酸和一水合氨是弱电解质,在溶液里部分电离,氢氧化钠是强电解质,完全电离,向混合溶液中滴加醋酸,醋酸先和氢氧化钠反应生成强电解质醋酸钠,氢氧化钠完全反应后,醋酸再和氨水反应生成强电解质醋酸铵,根据溶液中离子浓度变化与电导率的关系分析解答;
D、该反应为放热反应,反应物总能量应该高于生成物总能量.
B、该反应为放热反应,温度升高,平衡向着逆向移动,K逆中增大,而K正减小;
C、醋酸和一水合氨是弱电解质,在溶液里部分电离,氢氧化钠是强电解质,完全电离,向混合溶液中滴加醋酸,醋酸先和氢氧化钠反应生成强电解质醋酸钠,氢氧化钠完全反应后,醋酸再和氨水反应生成强电解质醋酸铵,根据溶液中离子浓度变化与电导率的关系分析解答;
D、该反应为放热反应,反应物总能量应该高于生成物总能量.
解答:
解:A、0.1mol?L-1NaOH溶液的pH为13,用0.1mol?L-1盐酸滴定恰好中和时pH为7,因浓度相同,则体积相同,但酸碱中和在接近终点时,pH会发生突变,曲线的斜率会很大,故A错误;
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K逆会增大,而K正会减小,图象中变化与实际上的变化不符,故B错误;
C、氢氧化钠是强电解质,氨水是弱电解质,滴加的弱电解质先和氢氧化钠反应生成强电解质醋酸钠,但溶液体积不断增大,溶液被稀释,所以电导率下降;当氢氧化钠完全被中和后,醋酸继续与弱电解质氨水反应生成强电解质醋酸铵,所以电导率增大;氨水也完全反应后,继续滴加醋酸,因为溶液被稀释,电导率有下降趋势,故C正确;
D、因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是反应物总能量低于生成物总能量,反应为吸热反应,故D错误;
故选C.
B、因反应为放热反应,则升高温度,平衡逆向移动,平衡后升温K逆会增大,而K正会减小,图象中变化与实际上的变化不符,故B错误;
C、氢氧化钠是强电解质,氨水是弱电解质,滴加的弱电解质先和氢氧化钠反应生成强电解质醋酸钠,但溶液体积不断增大,溶液被稀释,所以电导率下降;当氢氧化钠完全被中和后,醋酸继续与弱电解质氨水反应生成强电解质醋酸铵,所以电导率增大;氨水也完全反应后,继续滴加醋酸,因为溶液被稀释,电导率有下降趋势,故C正确;
D、因该反应是放热反应,应反应物的总能量大于生成物的总能量,但图象描述是反应物总能量低于生成物总能量,反应为吸热反应,故D错误;
故选C.
点评:本题以图象与中和滴定、化学平衡、溶液导电性与溶液离子浓度大小关系、反应中的能量变化来考查学生,这些知识点是新课程改革考查的重点,明确考点“形变神不变”,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在下列溶液中能大量共存的离子组是( )
| A、Fe3+、Na+、Cl-、SCN- | ||
B、HCO3-、Ca2+、C
| ||
| C、Na+、AlO2-、NO3-、H+ | ||
| D、K+、Na+、Cl-、SO42- |
某固体A在一定条件下加热分解,产物全是气体,A的分解反应为:2A
B↑+2C↑+2D↑,现测得分解产生的混合气体对氢气的相对密度为d,则A的相对分子质量为( )
| ||
| A、2d | B、10d |
| C、5d | D、0.8d |
 如图是某只含有C、H、O、N的有机物简易球棍模型.下列关于该有机物的说法正确的是( )
如图是某只含有C、H、O、N的有机物简易球棍模型.下列关于该有机物的说法正确的是( )| A、分子式为C3H7NO |
| B、在一定条件下,可以生成高分子化合物 |
| C、不能和盐酸溶液反应 |
| D、不能和NaOH溶液反应 |
设阿伏加德罗常数为NA,下列叙述中正确的是( )
| A、常温常压下,32克氧气中原子个数为NA |
| B、标准状况下,1mol H2O的体积为22.4L |
| C、常温常压下,1mol H2的质量为2克 |
| D、物质的量浓度为0.5mol/L的MgCl2溶液中,含有的Cl-数为NA |
常温下,有关下列4种溶液的说法正确的是( )
| ① | ② | ③ | ④ |
| 0.1mol?L-1氨水 | Ph=11 氨水 |
0.1mol?L-1 盐酸 |
pH=3 盐酸 |
| A、由水电离出的c(H+):③>① |
| B、①稀释到原来的100倍,pH与②相同 |
| C、①与③混合,若溶液pH=7,则溶液中c(NH4+)>C(Cl-) |
| D、②与④等体积混合,混合液pH>7 |
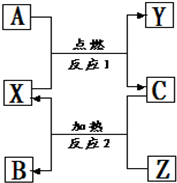 A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答:
A、B、C是中学化学常见的单质,X、Y、Z是中学化学常见的氧化物,它们之间有如右图所示的转化关系,请据图回答: 在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)
在①CO2、②NO2、③CO、④Cl2、⑤HCl、⑥NH3等气体中(选填序号)