题目内容
向蒸馏水中滴入少量稀盐酸后,下列说法正确的是( )
| A、c(H+)?c(OH-)比值不变 |
| B、溶液pH增大 |
| C、c(OH-)降低了 |
| D、水电离出的c(H+)增加了 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:A、向蒸馏水中滴入少量稀盐酸后,氢离子浓度增大,氢氧根离子浓度减小;
B、滴入少量盐酸,氢离子浓度变大;
C、c(H+)?c(OH-)乘积不变,根据氢离子浓度变化判断;
D、滴入少量盐酸,抑制H2O的电离.?
B、滴入少量盐酸,氢离子浓度变大;
C、c(H+)?c(OH-)乘积不变,根据氢离子浓度变化判断;
D、滴入少量盐酸,抑制H2O的电离.?
解答:
解:A、向蒸馏水中滴入少量稀盐酸后,氢离子浓度增大,氢氧根离子浓度减小,则
增大,故A错误;
B、滴入少量盐酸,氢离子浓度变大,溶液的pH减小,故B错误;
C、c(H+)?c(OH-)乘积不变,氢离子浓度变大,c(OH-)降低,故C正确;
D、滴入少量盐酸,抑制H2O的电离,水电离出的氢离子浓度减小,故D错误;
故选C.?
| c(H+) |
| c(OH-) |
B、滴入少量盐酸,氢离子浓度变大,溶液的pH减小,故B错误;
C、c(H+)?c(OH-)乘积不变,氢离子浓度变大,c(OH-)降低,故C正确;
D、滴入少量盐酸,抑制H2O的电离,水电离出的氢离子浓度减小,故D错误;
故选C.?
点评:本题考查水的离子积常数和水的电离平衡的移动,题目难度不大,注意温度不变时Kw=c(H+)?c(OH-)不变.

练习册系列答案
相关题目
将少量Na投入下列溶液中,既有气体又有沉淀析出的是( )
| A、NaCl |
| B、(NH4)2SO4 |
| C、CuSO4 |
| D、NH4HSO3 |
下列有关实验原理或操作的示意图合理的是( )
A、 制取蒸馏水 |
B、 收集氯化氢 |
C、 蒸发结晶 |
D、 实验室制取乙酸乙酯 |
为了除去括号中的杂质,所选用试剂不正确的是( )
| A、CO2(SO2):饱和NaHCO3溶液 |
| B、CO2(HCl):饱和NaHCO3溶液 |
| C、CO2(H2O):浓H2SO4 |
| D、Na2CO3溶液(NaHCO3):Ca(OH)2溶液 |
聚甲基丙烯酸甲酯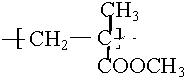 的单体与氢氧化钠共热后,当加入盐酸后能得到两种有机物,下列的哪一种物质与产物之一互为同分异构体( )
的单体与氢氧化钠共热后,当加入盐酸后能得到两种有机物,下列的哪一种物质与产物之一互为同分异构体( )
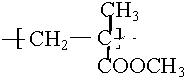 的单体与氢氧化钠共热后,当加入盐酸后能得到两种有机物,下列的哪一种物质与产物之一互为同分异构体( )
的单体与氢氧化钠共热后,当加入盐酸后能得到两种有机物,下列的哪一种物质与产物之一互为同分异构体( )| A、丁醇 | B、丁烯酸 |
| C、甲酸丙酯 | D、甲酸丙烯酯 |
现有下列一些萘的衍生物的结构简式,与①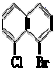 和②
和②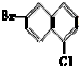 互为同分异构体的是( )
互为同分异构体的是( )
 和②
和② 互为同分异构体的是( )
互为同分异构体的是( )A、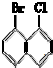 |
B、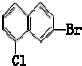 |
C、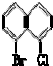 |
D、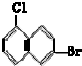 |
下列递变情况错误的是( )
| A、Na、Mg、Al最外电子层电子数依次增多 |
| B、P、S、Cl最高正价依次升高 |
| C、Li、Na、K金属性依次增强 |
| D、N、O、F最高正价依次升高 |
下列叙述中,正确的是( )
| A、生物质能来源于植物及其加工产品贮存的能量,不包括农业废弃物、动物粪便等 |
| B、密闭容器可逆反应N2+3H2?2NH3达到平衡后,增加氮气,氢气的转化率一定增大 |
| C、平衡常数发生变化,化学平衡必定发生移动,达到新平衡 |
| D、废弃的电池、金属制品属于不可回收再利用的资源 |
下列说法正确的是( )
| A、金属与盐溶液间的反应一定是置换反应 | ||||
| B、能与酸反应的氧化物一定是碱性氧化物 | ||||
C、
| ||||
| D、常见金属铁和铝在工业上是由热还原法制得的 |