题目内容
下列递变情况错误的是( )
| A、Na、Mg、Al最外电子层电子数依次增多 |
| B、P、S、Cl最高正价依次升高 |
| C、Li、Na、K金属性依次增强 |
| D、N、O、F最高正价依次升高 |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.根据Na、Mg、Al最外电子层电子数分析;
B.根据元素的最高正价等于核外最外层电子数分析;
C.同主族元素从上到下元素的金属性逐渐增强;
D.主族元素最高正价一般等于其最外层电子数,但氧元素、氟元素一般没有正化合价.
B.根据元素的最高正价等于核外最外层电子数分析;
C.同主族元素从上到下元素的金属性逐渐增强;
D.主族元素最高正价一般等于其最外层电子数,但氧元素、氟元素一般没有正化合价.
解答:
解:A.Na、Mg、Al最外电子层电子数分别为1、2、3,依次增多,故A正确;
B.P、S、Cl元素最外层电子数分别为5、6、7,最高正价分别为+5、+6、+7,最高正价依次升高,故B正确;
C.Li、Na、K在同一主族,从上到下元素的金属性逐渐增强,故C正确;
D.N最外电子层电子数为5,最高正价为+5,O、F一般不呈现正价,故D错误;
故选D.
B.P、S、Cl元素最外层电子数分别为5、6、7,最高正价分别为+5、+6、+7,最高正价依次升高,故B正确;
C.Li、Na、K在同一主族,从上到下元素的金属性逐渐增强,故C正确;
D.N最外电子层电子数为5,最高正价为+5,O、F一般不呈现正价,故D错误;
故选D.
点评:本题考查元素周期律,明确同主族、同周期元素的性质变化规律是解答本题的关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法或表示法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
| C、C(石墨)=C(金刚石)△H>0 所以石墨比金刚石稳定 |
| D、在101 kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
在NO2与水的反应中( )
| A、NO2既有被氧化的又有被还原的 |
| B、NO2在反应中只做了还原剂 |
| C、NO2在反应中只做了氧化剂 |
| D、NO2既是氧化剂又是还原剂 |
向蒸馏水中滴入少量稀盐酸后,下列说法正确的是( )
| A、c(H+)?c(OH-)比值不变 |
| B、溶液pH增大 |
| C、c(OH-)降低了 |
| D、水电离出的c(H+)增加了 |
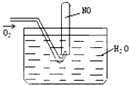 如图进行实验,试管内装有12mL NO,然后间歇而缓慢地通入8mL O2.下面有关实验最终状态的描述正确的是( )
如图进行实验,试管内装有12mL NO,然后间歇而缓慢地通入8mL O2.下面有关实验最终状态的描述正确的是( )| A、试管内气体呈棕红色 |
| B、试管内气体为无色的NO |
| C、试管内气体为无色的O2 |
| D、试管内液面高度上升到试管底部 |
向体积为VaL浓度为0.05mol?L-1CH3COOH溶液中加入体积为Vb L浓度为0.05mol?L-1KOH溶液,下列关系错误的是( )
| A、Va>Vb时:c (CH3COOH)+c (CH3COO-)>c (K+) |
| B、Va=Vb时:c (CH3COOH)+c (H+)=c (OH-) |
| C、Va<Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) |
| D、Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
已知298K时,N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol,在相同条件下向密闭容器中加入1molN2和3molH2,达到平衡时的反应热为△H1,向另一容积相同的密闭容器中通入0.95molN2、2.85molH2、0.1molNH3,达到平衡时的反应热为△H2,则下列关系正确的是( )
| A、△H1=△H2=-92.4 kJ/mol |
| B、-92.4 kJ/mol<△H1<△H2 |
| C、△H1<△H2<-92.4 kJ/mol |
| D、△H1=△H2<-92.4 kJ/mol |
下列有关工业生产的叙述正确的是( )
| A、接触法制硫酸中采用沸腾炉的目的是为了使硫磺或黄铁矿燃烧充分,提高原料的利用率 |
| B、合成氨生产过程中采用高温高压条件都是为了提高N2、H2的转化率 |
| C、硫酸工业中,在接触室安装热交换器是为了利用硫磺或黄铁矿燃烧时放出的热量 |
| D、在联合制碱法中,参与循环的物质有CO2和NH3 |
下列叙述正确的是( )
| A、同系物可能互为同分异构体 |
| B、甲烷化学性质比较稳定,不能被任何氧化剂氧化 |
| C、甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3还是CCl4,都属于取代反应 |
| D、C4H10分子中四个碳原子在一条直线上 |