题目内容
10.自热诗篇已成为现代生活的时尚.自热食品包装中有两包发热剂,在这两包发热剂中最适合盛饭的物质是( )| A. | 熟石灰和水 | B. | 生石灰和水 | ||
| C. | 氯化钠和水 | D. | 氯化铵和氢氧化钡晶体 |
分析 最适合盛饭的物质,也就是在化学变化过程中有热量放出的反应;
A、熟石灰溶于水放出热量较小;
B、生石灰溶于水反应生成熟石灰同时放出大量的热量;
C、氯化钠溶于水既不吸热也不放热,温度基本保持不变;
D、氯化铵和氢氧化钡晶体反应吸热,温度降低.
解答 解:最适合盛饭的物质,也就是在化学变化过程中有热量放出的反应;
A、熟石灰溶于水放出热量较小,不太适合盛饭,故A错误;
B、生石灰溶于水反应生成熟石灰同时放出大量的热量,温度升高,适合盛饭,故B正确;
C、氯化钠溶于水既不吸热也不放热,温度基本保持不变,不适合盛饭,故C错误;
D、氯化铵和氢氧化钡晶体反应吸热,温度降低,不适合盛饭,故D错误;
故选B.
点评 本题考查发热剂的选择,实际考查常见的放热反应,吸热反应的判断,本题难度中等.

练习册系列答案
相关题目
1.阅读表短周期主族元素的相关信息:
请回答:
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图: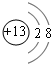 .
.
(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”化合物).
(5)C元素形成的单质能与A的最高价氧化物对应的水化物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的简单离子半径简单最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |
(1)写出E在元素周期表中的位置:第二周期第ⅣA族;C的简单离子的结构示意图:
 .
.(2)X的化学式为NaClO.
(3)A、B、C三种元素的简单离子的半径由大到小的顺序为O2->Na+>Al3+(用离子符号表示).
(4)A、B两元素组成的化合物A2B2属于离子化合物(填“离子”或“共价”化合物).
(5)C元素形成的单质能与A的最高价氧化物对应的水化物反应,其离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
18.表是元素周期表的一部分,针对表中的①~⑧种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:氩.
(2)在这些元素中,属于金属的是:Na、Al.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)最高价氧化物的水化物显两性的是氢氧化铝;写出它与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)在这些元素中,属于金属的是:Na、Al.
(3)在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4.
(4)最高价氧化物的水化物显两性的是氢氧化铝;写出它与盐酸反应的离子方程式Al(OH)3+3H+=Al3++3H2O.
5.下列变化中,需要吸收热量用于克服分子间作用力的是( )
| A. | 干冰置于空气中升华 | B. | 加热使石英熔化 | ||
| C. | 将食盐溶解于水 | D. | 加热使硫化氢分解 |
15.下列各组顺序的排列不正确的是( )
| A. | 熔点:金刚石>干冰 | B. | 离子半径:O2->Na+ | ||
| C. | 碱性:KOH>Al(OH)3 | D. | 稳定性:SiH4>H2S |
2.下列有关实验基本操作或现象的描述不正确的是( )
| A. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| B. | 溶剂蒸发的速率越快,或浓缩后的溶液冷却得越快,析出的晶体颗粒就越大 | |
| C. | 油脂在热NaOH溶液中完全水解后加入饱和食盐水,可观察到液面上有固体析出 | |
| D. | 制备NaCl晶体时,晶体表面含有少量KNO3,用水淋洗后可得到较纯净的NaC1 |
19.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述错误的是( )
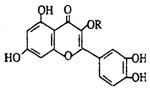

| A. | 可溶于有机溶剂 | B. | 分子中有三个苯环 | ||
| C. | 1mol维生素P可以和6molBr2反应 | D. | 1mol维生素P可以和4molNaOH反应 |


