题目内容
取10.4g某醇与冰醋酸进行酯化反应,生成11.6g的酯,同时回收到未反应的醇3g,则醇可能是( )
| A、乙醇 | B、丁醇 | C、苯甲醇 | D、辛醇 |
考点:化学方程式的有关计算
专题:计算题
分析:选项中都是一元醇,令醇为R-OH,与乙酸发生反应:CH3COOH+HO-R
CH3COOR+H2O,参加反应的醇、乙酸与生成的酯、水的物质的量都相等,假设物质的量都是xmol,根据质量守恒定律列方程,再计算醇的摩尔质量进行判断.
| 浓硫酸 |
| △ |
解答:
解:选项中都是一元醇,令醇为R-OH,与乙酸发生反应:CH3COOH+HO-R
CH3COOR+H2O,参加反应的醇、乙酸与生成的酯、水的物质的量都相等,假设物质的量都是xmol,
参加反应醇的质量=10.4g-3g=7.4g,
根据质量守恒定律:7.4+60x=11.6+18x
解得x=0.1,
故该醇的摩尔质量=
=74g/mol,
乙醇的摩尔质量为46g/mol、丁醇的摩尔质量为74g/mol、苯甲醇的摩尔质量为108g/mol,辛醇的摩尔质量为130g/mol,故丁醇符合,
故选B.
| 浓硫酸 |
| △ |
参加反应醇的质量=10.4g-3g=7.4g,
根据质量守恒定律:7.4+60x=11.6+18x
解得x=0.1,
故该醇的摩尔质量=
| 7.4g |
| 0.1mol |
乙醇的摩尔质量为46g/mol、丁醇的摩尔质量为74g/mol、苯甲醇的摩尔质量为108g/mol,辛醇的摩尔质量为130g/mol,故丁醇符合,
故选B.
点评:本题考查化学方程式计算、酯化反应,难度不大,判断各物质的物质的量关系是关键.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列离子方程式正确的是( )
A、碳酸钙中加入盐酸 C
| ||
| B、氢氧化钡与稀硫酸反应 OH-+H+=H2O | ||
C、碳酸钠溶于醋酸溶液 C
| ||
| D、氯化铁溶液与铜反应 Fe3++Cu=Fe2++Cu2+ |
下列物质中,不与盐酸反应,但可与氢氧化钠溶液反应的是( )
| A、Al(OH)3 |
| B、Al2O3 |
| C、SiO2 |
| D、Al |
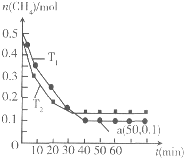 工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )| A、T1>T2 |
| B、b>0 |
| C、K(T1)>K(T2) |
| D、a点时NO2的转化率为33.3% |
下列各对物质中,互为同系物的是( )
A、 |
| B、HCOOCH3与CH3CHOOH |
C、 |
| D、C6H5OH与C6H5CH2OH |
中国科学院在世界上首次发现铂元素的一种同位素
Pt,它的中子数为( )
202 78 |
| A、78 | B、124 |
| C、202 | D、280 |
短周期元素A和B可形成AB3型化合物.若B原子序数为m,则A的原子序数为下面算式中的①m+6 ②m+4 ③m-4 ④m-2 ⑤m+8 ⑥m+14 ⑦m-12( )
| A、②③⑥ | B、①②③④ |
| C、①②⑥⑦ | D、①②③④⑤⑥⑦ |
下列关于金属保护的说法不正确的是( )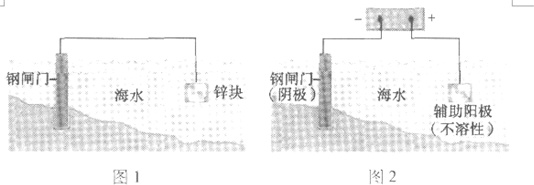

| A、图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法 |
| B、两种保护法共同点是被保护的钢闸门上均为电子流出 |
| C、图1中的负极反应是Zn-2e-═Zn2+ |
| D、图2中钢闸门表面发生还原反应 |
反应Br+H2?HBr+H的能量对反应历程的关系如图甲.下述中不正确的是( )


| A、该反应的正反应是吸热反应 |
| B、加入催化剂,该化学反应的反应热不变 |
| C、加入催化剂可降低正反应的活化能,同时增大逆反应的活化能 |
| D、加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |