题目内容
下列关于金属保护的说法不正确的是( )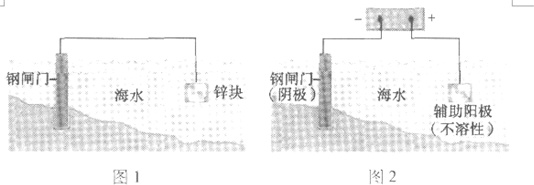

| A、图1是牺牲阳极阴极保护法,图2是外加电流阴极保护法 |
| B、两种保护法共同点是被保护的钢闸门上均为电子流出 |
| C、图1中的负极反应是Zn-2e-═Zn2+ |
| D、图2中钢闸门表面发生还原反应 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:A.牺牲阳极的阴极保护法指的是原电池的负极金属易被腐蚀,而正极金属被保护的原理,使用外加电流的阴极保护法说明该该金属防腐的措施中连接外加电源,且阴极连接电源负极;
B.两种保护法共同点是被保护的钢闸门上均没有电子流出;
C.图1中的负极是活泼金属锌;
D.图2中钢闸门作电解池的阴极.
B.两种保护法共同点是被保护的钢闸门上均没有电子流出;
C.图1中的负极是活泼金属锌;
D.图2中钢闸门作电解池的阴极.
解答:
解:A.钢闸门连接锌块,Fe、Zn、电解质溶液构成原电池,Fe失电子能力小于Zn而作正极被保护,所以该保护方法属于牺牲阳极的阴极保护法,水中的钢闸门连接电源负极,阴极上得电子被保护,所以属于使用外加电流的阴极保护法,故A正确;
B.钢闸门连接锌块,Zn为原电池负极电子流出,水中的钢闸门连接电源负极,阴极上得电子被保护,辅助阳极失去电子,故B错误;
C.Fe、Zn、电解质溶液构成原电池,Fe失电子能力小于Zn,负极反应是Zn-2e-═Zn2+,故C正确;
D.水中的钢闸门连接电源负极,阴极上得电子被保护,发生还原反应,故D正确;
故选B.
B.钢闸门连接锌块,Zn为原电池负极电子流出,水中的钢闸门连接电源负极,阴极上得电子被保护,辅助阳极失去电子,故B错误;
C.Fe、Zn、电解质溶液构成原电池,Fe失电子能力小于Zn,负极反应是Zn-2e-═Zn2+,故C正确;
D.水中的钢闸门连接电源负极,阴极上得电子被保护,发生还原反应,故D正确;
故选B.
点评:本题考查了金属的腐蚀与防护,注意理解各种防腐方法的原理是解题关键,题目难度不大.

练习册系列答案
相关题目
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、常温常压下24g 金属镁变成Mg2+失去电子2NA |
| C、标准状况下,22.4LH2O含有氢原子个数为2NA |
| D、11.2L氢气一定含有NA 个氢原子 |
取10.4g某醇与冰醋酸进行酯化反应,生成11.6g的酯,同时回收到未反应的醇3g,则醇可能是( )
| A、乙醇 | B、丁醇 | C、苯甲醇 | D、辛醇 |
下列说法中正确的是( )
| A、烃是指只含有碳、氢元素的有机物 |
| B、燃烧后能产生CO2和H2O的有机物一定是烃 |
| C、天然气、沼气、坑气、煤气的主要成分都是甲烷 |
| D、形成化合物种类最多的元素位于周期表中第二周期第VA族 |
如图是某硫酸试剂瓶的标签上的部分信息.下列说法正确的是( )


| A、常温下,该试剂可与金属铝反应生成大量的无色气体 |
| B、1 mol Zn与足量的该硫酸反应生成2 g氢气 |
| C、该硫酸与等体积水混合所得溶液的物质的量浓度大于9.2 mol/L |
| D、向50 mL该硫酸中加入足量的铜片,加热,反应后被还原的硫酸的物质的量小于0.46 mol |
下列有关合金的叙述中正确的是( )
①合金具有金属特性;②合金中的元素的化合价为零;③合金中不一定含有金属元素;④钢是铁合金;⑤合金属于金属材料;⑥生铁可完全溶解于稀盐酸.
①合金具有金属特性;②合金中的元素的化合价为零;③合金中不一定含有金属元素;④钢是铁合金;⑤合金属于金属材料;⑥生铁可完全溶解于稀盐酸.
| A、①②③④⑤⑥ | B、①③④⑤⑥ |
| C、①②④⑤ | D、①④⑥ |
一定温度下,满足下列条件的溶液一定呈酸性的是( )
| A、pH<7的某物质的水溶液 |
| B、加酚酞后显无色的溶液 |
| C、能与金属Al反应放出H2的溶液 |
| D、c(H+)>c(OH-)的任意物质的水溶液 |
下列各组中的性质比较,正确的是( )
| A、酸性HClO4>HBrO4>HIO4 |
| B、碱性NaOH>Mg(OH)2>Ca(OH)2 |
| C、C、N、O、F的最高正价依次升高 |
| D、氧化性:Na+>Mg2+>Al3+ |
下列物质中,属于乙醇同系物的是( )
A、 |
B、 |
| C、CH2OHCH2OH |
| D、(CH3)2CHOH |