题目内容
下列离子方程式不正确的是( )
| A、向碳酸氢钠溶液滴加NaOH溶液 HCO3-+OH-=CO32-+H2O |
| B、MgO溶于盐酸中:O2-+2H+=H2O |
| C、镁和稀硫酸反应 Mg+2H+=Mg2++H2↑ |
| D、氯气与水反应 Cl2+H2O?2H++Cl-+ClO- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸氢钠溶液滴加NaOH溶液反应生成碳酸钠和水;
B.氧化物在水溶液里中不电离,保留化学式;
C.镁和稀硫酸反应生成硫酸镁和氢气;
D.次氯酸为弱电解质不能拆.
B.氧化物在水溶液里中不电离,保留化学式;
C.镁和稀硫酸反应生成硫酸镁和氢气;
D.次氯酸为弱电解质不能拆.
解答:
解:A.碳酸氢钠溶液滴加NaOH溶液反应的离子方程式为HCO3-+OH-=CO32-+H2O,故A正确;
B.MgO溶于盐酸中反应的离子方程式为MgO+2H+=H2O+Mg2+,氧化物在水中不能电离,应该保留化学式,故B错误;
C.镁和稀硫酸反应离子方程式为Mg+2H+=Mg2++H2↑,故C正确;
D.氯气与水反应离子方程式:Cl2+H2O?H++Cl-+HClO,故D错误;
故选:BD.
B.MgO溶于盐酸中反应的离子方程式为MgO+2H+=H2O+Mg2+,氧化物在水中不能电离,应该保留化学式,故B错误;
C.镁和稀硫酸反应离子方程式为Mg+2H+=Mg2++H2↑,故C正确;
D.氯气与水反应离子方程式:Cl2+H2O?H++Cl-+HClO,故D错误;
故选:BD.
点评:书写离子方程式,化学式的拆分是难点,本题BD两选项均是化学式拆分错误,注意在离子方程式中,强酸强碱和易溶性的盐拆分成离子形式,难溶物、弱电解质、单质、氧化物、沉淀、气体、非电解质均保留化学式.

练习册系列答案
相关题目
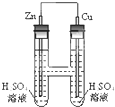 如图所示,下列叙述正确的是( )
如图所示,下列叙述正确的是( )| A、过程中溶液的PH会减小 |
| B、锌为正极,发生氧化反应 |
| C、铜棒上反应为2H++2e=H2↑ |
| D、电流方向从Zn经导线到Cu |
下列各物质与其用途对应不正确的是( )
| A、钾钠合金--快中子反应堆热交换剂 |
| B、硫酸钡--钡餐、白色颜料等 |
| C、二氧化硅--光导纤维、半导体材料 |
| D、硫酸铜--净水、治疗鱼类皮肤病 |
可逆反应N2+3H2?2NH3;△H<0.当单独改变下列条件后,有关叙述中错误的是( )
| A、体积不变,加入氩气,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
| B、加入催化剂,v正、v逆都发生变化,且变化的倍数相同 |
| C、压缩体积,增大压强时,v正、v逆都增大,且v正增大倍数大于v逆增大倍数 |
| D、降低温度时,v正、v逆都减小,且v正减小倍数小于v逆减小倍数 |
元素周期表中第116号元素已由俄罗斯科学家找到.假设第116号元素的元素符号为R,则下列有关叙述中不正确的是( )
①R的非金属性比S强
②R元素原子的内层电子共有110个
③R是过渡金属元素
④R元素原子的最高价氧化物对应的水化物为强酸
⑤R元素的最高价氧化物的化学式为RO3.
①R的非金属性比S强
②R元素原子的内层电子共有110个
③R是过渡金属元素
④R元素原子的最高价氧化物对应的水化物为强酸
⑤R元素的最高价氧化物的化学式为RO3.
| A、①③④ | B、①②④ |
| C、③④ | D、②⑤ |
下列有关实验操作不正确的是( )
| A、蒸发操作时,应在混合物中有晶体析出时立即停止加热 |
| B、在萃取实验中,萃取剂要求与原溶剂互不相溶,且溶质在萃取剂中的溶解度更大 |
| C、开始蒸馏时,应该先开冷凝水,再加热;蒸馏完毕,应该先撤酒精灯再关冷凝水 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
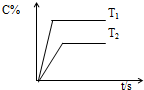 对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )
对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )| A、T1>T2,△H>0 |
| B、T1>T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1<T2,△H<0 |
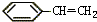 ,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )