题目内容
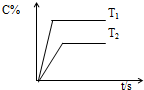 对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )
对于达到平衡的反应:A(g)+B(g)?C(g),符合图中所示结论的是( )| A、T1>T2,△H>0 |
| B、T1>T2,△H<0 |
| C、T1<T2,△H>0 |
| D、T1<T2,△H<0 |
考点:体积百分含量随温度、压强变化曲线
专题:化学平衡专题
分析:由图可知T1时到达平衡所用时间短,则温度T1>T2,温度高时C的百分含量高,根据升温平衡向吸热方向移动来分析.
解答:
解:由图可知T1时到达平衡所用时间短,说明T1温度下反应速率快,则温度T1>T2,已知T1时C的百分含量大于T2时C的百分含量,说明温度越高,C的百分含量越大,即升高温度平衡正移,所以正方向为吸热反应,即△H>0;
故选A.
故选A.
点评:本题考查了化学平衡的图象,注意把握图象中拐点的含义,以及影响速率和平衡的因素是解决本题的关键,题目难度不大.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
下列离子方程式不正确的是( )
| A、向碳酸氢钠溶液滴加NaOH溶液 HCO3-+OH-=CO32-+H2O |
| B、MgO溶于盐酸中:O2-+2H+=H2O |
| C、镁和稀硫酸反应 Mg+2H+=Mg2++H2↑ |
| D、氯气与水反应 Cl2+H2O?2H++Cl-+ClO- |
下列化学反应不属于氧化还原反应的是( )
| A、Zn+2HCl═ZnCl2+H2↑ | ||||
| B、BaCl2+H2SO4═BaSO4↓+2HCl | ||||
C、H2+CuO
| ||||
| D、Fe+CuSO4═FeSO4+Cu |
下列说法正确的是( )
| A、物质的化学变化都伴随着能量变化 |
| B、凡是吸热反应都需要加热 |
| C、任何反应中的能量变化都表现为热量变化 |
| D、拆开旧化学键吸收的能量一定大于形成新化学键放出的能量 |
在一定的温度下,可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A、A、B、C的分子数相等 |
| B、A、B、C的浓度不再变化 |
| C、单位时间生成n mol A,同时生成2n mol C |
| D、A、B、C的分子数之比为1:3:2 |
下列有关电解饱和食盐水的叙述错误的是( )
| A、与电源负极相连的铁丝圈叫阴极 |
| B、与电源正极相连的石墨棒叫阳极 |
| C、随着电解的进行,阳极附近溶液的pH显著升高 |
| D、阳极放出的气体能使湿润的淀粉碘化钾试纸变蓝 |
下列物质在水溶液中的电离方程式书写完全正确的是( )
| A、H2SO4═H++SO42- |
| B、Al2(SO4)3=2Al3++3SO42- |
| C、KClO3=K++3O2-+Cl5+ |
| D、NaHSO4=Na++HSO4- |
下列关于浓硫酸与浓硝酸的叙述中不正确的是( )
| A、都是常用的干燥剂 |
| B、一定条件下都能与铜等金属反应 |
| C、常温下都可以储存于铝制槽罐中 |
| D、敞口露置于空气中,一段时间后,容器内的溶质的物质的量浓度都降低 |