题目内容
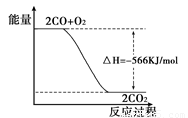
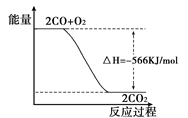
已知:2 CO(g) + O2(g) = 2CO2(g) △H=-566kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-802kJ/mol
H2O(g)= H2O(l) △H=-44KJ/mol
则CH4在空气中不完全燃烧时,热化学方程式是
A.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) △H=-1038kJ/mol
B.4CH4(g)+7O2(g)=2CO2(g)+2CO(g)+8H2O(l) △H=-2642kJ/mol
C.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(g) △H=-1497kJ/mol
D.2CH4(g)+3.5O2(g)=CO2(g)+CO(g)+4H2O(l) △H=-1497kJ/mol
D

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
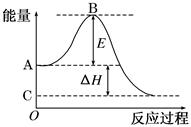
已知:2 CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ/mol根据以上热化学方程式判断,下列说法错误的是
| A.CO2气体分解生成CO气和O2气体的反应是放热反应 |
| B.CO气体与O2气体生成CO2气体的反应是放热反应 |
| C.上图可表示由CO气体生成CO2气体的反应过程和能量关系 |
| D.在相同条件下,2 mol CO气体与1 mol O2气体的能量总和大于2 mol CO2气体的能量 |
 2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题:
2CO2(g)反应过程的能量变化如图所示。已知1 mol CO (g)氧化为1 mol CO2 (g)的ΔH =-283 kJ/mol。请回答下列问题: