题目内容
6.向100mL 1mol•L-1的NaOH溶液中通入一定量SO2后,将所得溶液蒸干得到5.8g固体物质,则该固体的成分是( )| A. | Na2SO3 | B. | NaHSO3 | C. | Na2SO3、NaHSO3 | D. | Na2SO3、NaOH |
分析 若固体全为Na2SO3,根据Na元素守恒计算Na2SO3的质量;
若固体全为NaHSO3,根据Na元素守恒计算NaHSO3的质量;
若固体Na2SO3与NaHSO3的混合物,则其质量在NaHSO3的质量与Na2SO3的质量之间.
解答 解:n(NaOH)=0.1L×1mol/L=0.1 mol,
若固体全为Na2SO3,由Na元素守恒可知,Na2SO3的质量为:$\frac{0.1mol}{2}$×126g/mol=6.3g;
若固体全为NaHSO3,由Na元素守恒可知,NaHSO3的质量为:0.1mol×104g/mol=10.4g;
而5.8g<6.3g,故固体成分为Na2SO3与NaOH,
故选D.
点评 本题考查混合物有关计算,注意利用极限法进行解答,侧重考查学生分析计算能力,难度中等.

练习册系列答案
相关题目
1.欲使FeCl2(含少量HCl)转化为FeCl3,而又不引入其他杂质离子,可加入( )
| A. | KMnO4 | B. | Cl2 | C. | HNO3 | D. | H2O2 |
11.下列有关结构的说法正确的是( )
| A. | 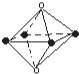 是从NaCl晶体结构图中分割出来的部分结构. 是从NaCl晶体结构图中分割出来的部分结构. | |
| B. | 钡在氧气中燃烧得到一种晶体,其结构如图所示,则该晶体的化学式为Ba2O2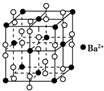 | |
| C. | SiCl4是非极性分子,分子中Si原子处在4个Cl原子所组成的正方形的中心 | |
| D. | 白磷(P4)和甲烷都是正四面体型分子,但分子中的共价键数目和键角均不同 |
19.下列变化属于氧化还原反应的是( )
| A. | 馒头在咀嚼过程中产生甜味 | |
| B. | 三氯化铁溶液长期放置产生红褐色固体 | |
| C. | 蛋白质溶液中加入饱和硫酸铵溶液,析出沉淀 | |
| D. | 植物油长期放置发生“酸败产生刺激性气味” |
20.下列反应属于吸热反应的是( )
| A. | 氢氧化钡与盐酸溶液反应 | B. | 葡萄糖在人体内氧化分解 | ||
| C. | 石灰石在高温下的分解反应 | D. | 锌粒与稀H2SO4反应制取H2 |