题目内容
16.相同质量的SO2和SO3(1)分子数目之比为5:4
(2)含氧原子个数比为5:6
(3)含有原子总数之比为15:16.
分析 根据n=$\frac{m}{M}$可知,等质量的二氧化硫和三氧化硫的物质的量之比与其摩尔质量成反比,据此计算出相同质量的SO2和SO3的物质的量之比;根据N=nNA可知,分子数、原子数与物质的量成正比,据此分别计算出二者分子数之比、含有氧原子个数之比及含有原子总数之比.
解答 解:根据n=$\frac{m}{M}$可知,等质量的二氧化硫和三氧化硫的物质的量之比与其摩尔质量成反比,则相同质量的SO2和SO3的物质的量之比=80g/mol:64g/mol=5:4,
(1)根据N=nNA可知,二者含有分子数目之比=5:4,
故答案为:5:4;
(2)相同质量的SO2和SO3分子中含有氧原子个数之比=(5×2):(4×3)=5:6,
故答案为:5:6;
(3)相同质量的SO2和SO3分子中含有原子总数之比=(5×3):(4×4)=15:16,
故答案为:15:16.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数之间的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的化学计算能力.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
6.19世纪中叶,门捷列夫总结出元素化学性质变化情况,门捷列夫的突出贡献是( )
| A. | 提出原子学说 | B. | 提出分子学说 | ||
| C. | 发现元素周期律 | D. | 发现能量守恒定律 |
7.下列反应中,属于氧化还原反应的是( )
| A. | Na2O+H2O═2NaOH | B. | 2Na2O2+2CO2═2Na2CO3+O2 | ||
| C. | Na2CO3+2HCl═2NaCl+CO2↑+H2O | D. | 2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O |
4.瓦斯中甲烷与氧气的质量比为1:4时极易爆炸,则下列说法正确的是( )
| A. | 此时甲烷与氧气的体积比为2:1 | |
| B. | 此时混合气体的平均相对分子质量约为26.7 | |
| C. | 此时混合气体中C、H、O原子的个数比为1:4:2 | |
| D. | 应在较为密闭的环境中使用瓦斯炉 |
11.1.28g某气体含有的分子数目为1.204×1022,则该气体的摩尔质量为( )
| A. | 64g | B. | 64 | C. | 64g/mol | D. | 32g/mol |
5.下列叙述中不正确的是( )
| A. | 共价化合物中,一定含非金属元素 | |
| B. | 共价化合物中,一定没有离子键 | |
| C. | 离子化合物中可能含有共价键 | |
| D. | 离子化合物中一定含有金属元素和非金属元素 |
12.关于如图各装置图的叙述不正确的是( )
| A. | 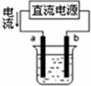 用如图装置精炼铜,a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 | |
| B. | 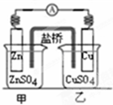 如图装置的盐桥中KCl的Cl-移向乙烧杯 | |
| C. |  如图装置中钢闸门应与外接电源的负极相连获得保护 | |
| D. | 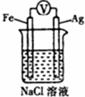 装置中滴入2滴黄色K3[Fe(CN)6]溶液,溶液中可能出现蓝色沉淀 |
9.下列反应属于氮的固定的是( )
| A. | 空气在雷电作用下所产生NO | |
| B. | NO和O2生成NO2 | |
| C. | NH4Cl与Ca(OH)2反应生成NH3 | |
| D. | 在加压降温的条件下使空气中的氮气液化 |
10.某混合溶液由两种或三种物质溶于水制成,且在溶液中一定满足如下关系:c(K+)=c(Cl-),c(Na+)=2c(SO42-).则溶质可能是( )
| A. | KCl、Na2SO4 | B. | KCl、Na2SO4、NaCl | ||
| C. | NaCl、Na2SO4、K2SO4 | D. | KCl、K2SO4、Na2SO4 |