题目内容
5.下列说法不正确的是( )
| A. | 将浓度为0.1 mol•L-1 HF溶液加水不断稀释过程中,K(HF)保持不变 | |
| B. | 等物质的量浓度的 NH4HSO4溶液和NaOH溶液等体积混合,溶液中各离子浓度大小关系为:c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 已知298K时氢氰酸(HCN)的Ka=4.9×10-10、碳酸的Ka1=4.4×10-7,Ka2=4.7×10-11,据此可推测将氢氰酸加入到碳酸钠溶液中能观察到有气泡产生 | |
| D. | 某温度下,相同体积、相同pH的盐酸和醋酸溶液分别加水稀释,pH随溶液体积V变化的曲线如图所示.II为醋酸稀释时pH的变化曲线,且a、b两点水的电离程度:a<b |
分析 A.电离常数只与温度有关;
B.等物质的量浓度的 NH4HSO4溶液和NaOH溶液等体积混合生成等浓度的硫酸铵和硫酸钠;
C.相同温度、浓度下,酸的电离平衡常数越大,酸的酸性越强,其酸根离子的水解能力越小,结合强酸制取弱酸分析解答;
D.醋酸为弱酸,存在电离平衡,当加水稀释时,氢离子浓度减小较慢,以此判断醋酸稀释时,pH的变化曲线;氢离子浓度越大,对水的电离的抑制程度越大.
解答 解:A.电离常数只与温度有关,将浓度为0.1 mol•L-1 HF溶液加水不断稀释过程中,K(HF)保持不变,故A正确;
B.等物质的量浓度的 NH4HSO4溶液和NaOH溶液等体积混合生成等浓度的硫酸铵和硫酸钠,铵根离子水解溶液显酸性,则c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-),故B正确;
C.酸性H2CO3>HCN>HCO3-,所以氢氰酸加入到碳酸钠溶液中,没有气体生成,故C错误;
D.醋酸为弱酸,存在电离平衡,当加水稀释时,氢离子浓度减小较慢,所以醋酸稀释时,pH增大较慢,曲线Ⅱ为醋酸的pH值变化;氢离子浓度越大,对水的电离的抑制程度越大,且a中溶液的pH小,即氢离子浓度大,所以a点水的电离程度小,则a、b两点水的电离程度:a<b,故D正确;
故选C.
点评 本题考查了弱电解质的电离,明确酸的电离平衡常数与酸性强弱、酸根离子水解能力的关系是解本题关键,难度中等.

练习册系列答案
相关题目
9.“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说法正确的是( )
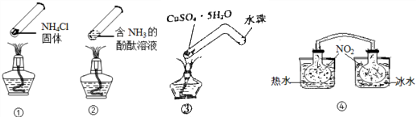

| A. | 加热时,①上部汇集了固体NH4Cl,说明NH4Cl易升华 | |
| B. | 加热时,②溶液颜色变,冷却后又恢复为原来的颜色 | |
| C. | 加热时,③中固体由蓝色变为白色,冷却后又恢复为原来的颜色 | |
| D. | ④中,浸泡在热水中的容器内气体颜色变深,说明受热时反应2NO2?N2O4向正方向移动 |
16.设NA为阿佛加德罗常数,下列对于0.3mol/L的K2SO4溶液的说法中正确的是( )
| A. | 溶液中含有0.6NA个K+ | |
| B. | 1L溶液中含有K+和SO42-总数为0.9NA | |
| C. | 取出10mL该溶液中,K+浓度为0.3mol/L | |
| D. | 100mL溶液中含有SO42-数目为0.6NA |
13.用NA表示阿伏伽德罗常数的值,下列判断正确的是( )
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 常温常压下,1.06gNaCO3含有的分子数目为0.02NA | |
| D. | 1L1mol/L的KClO3溶液中含有的Cl-个数为NA |
17.下列反应既是氧化还原反应,又是吸热反应是( )
| A. | 实验室制备氢气 | |
| B. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 | |
| C. | 灼热的木炭与CO2的反应 | |
| D. | 铝粉与氧化铁粉末反应 |
14.雾霾天气严重影响人们的生活,氮氧化物和硫氧化物是造成雾霾的主要原因之一.
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
(1)某同学测得该样本所含水溶性无机离子的化学组分及其平均浓度列出下表:(若缺少的离子用H+或OH-补充):
根据表中数据判断该试样的pH=4;该表有一处笔误,请你指正表中用亚硫酸根离子表示浓度有错,应用亚硫酸氢根离子表示.
Ⅱ.消除氮氧化物和硫化物有多种方法.
【方法一】:工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4(连二亚硫酸钠)和NH4NO3 产品的流程图如图(Ce为铈元素):

(2)装置Ⅰ中的主要反应的离子方程式为SO2+OH-=HSO3-.
(3)装置Ⅲ可以使Ce4+中再生,若用甲烷燃烧电池电解该装置中的溶液,当消耗24g甲烷时,理论上可再生12mol Ce4+.
(4)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,
该温度下,吸收液中c(Ca2+)一直保持为0.70mol/L,已知Ksp(CaSO3)=1.4×10-7.求吸收液中的SO32-的浓度2.0×10-7mol/L.(结果保留2位有效数字)
【方法二】:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图所示:

(5)图乙是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为Mn、200℃左右.
(6)用Fe做催化剂时,在氨气足量的情况下,不同$\frac{c(N{O}_{2})}{c(NO)}$=1:1脱氢效果最佳.已知生成11.2L N2(标)反应放出的热量为QkJ,此时对应的脱氢反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-4QkJ•mol-1.
【方法二】用活性炭还原法可以处理氮氧化物.
反应原理:1/2C(s)+NO(g)═1/2N2(g)+1/2CO2(g)△H=-QkJ/mol在T1℃时,反应进行到不同的时间测得各物质的浓度如下:
(7)T1℃时,该反应的平衡常数K=0.75.
(8)30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是通入一定量的NO或适当缩小容器的体积或增大压强或通入等物质的量的CO2和N2.
Ⅰ.将PM2.5样本用蒸馏水处理制成待测试样.
(1)某同学测得该样本所含水溶性无机离子的化学组分及其平均浓度列出下表:(若缺少的离子用H+或OH-补充):
| 离子 | K+ | Na+ | NH4+ | SO32- | NO3- | Cl- |
| 浓度/mol•L-1 | 7×10-6 | 3×10-6 | 2×10-5 | 3×10-5 | 5×10-5 | 2×10-5 |
Ⅱ.消除氮氧化物和硫化物有多种方法.
【方法一】:工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4(连二亚硫酸钠)和NH4NO3 产品的流程图如图(Ce为铈元素):

(2)装置Ⅰ中的主要反应的离子方程式为SO2+OH-=HSO3-.
(3)装置Ⅲ可以使Ce4+中再生,若用甲烷燃烧电池电解该装置中的溶液,当消耗24g甲烷时,理论上可再生12mol Ce4+.
(4)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,
该温度下,吸收液中c(Ca2+)一直保持为0.70mol/L,已知Ksp(CaSO3)=1.4×10-7.求吸收液中的SO32-的浓度2.0×10-7mol/L.(结果保留2位有效数字)
【方法二】:NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图所示:

(5)图乙是不同催化剂Mn和Cr在不同温度下对应的脱氢率,由图综合考虑可知最佳的催化剂和相应的温度分别为Mn、200℃左右.
(6)用Fe做催化剂时,在氨气足量的情况下,不同$\frac{c(N{O}_{2})}{c(NO)}$=1:1脱氢效果最佳.已知生成11.2L N2(标)反应放出的热量为QkJ,此时对应的脱氢反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-4QkJ•mol-1.
【方法二】用活性炭还原法可以处理氮氧化物.
反应原理:1/2C(s)+NO(g)═1/2N2(g)+1/2CO2(g)△H=-QkJ/mol在T1℃时,反应进行到不同的时间测得各物质的浓度如下:
| 时间(min) 浓度(mol/L-1) | 0min | 10min | 20min | 30min | 40min | 50min |
| NO(mol/L-1) | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2(mol/L-1) | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2(mol/L-1) | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
(8)30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是通入一定量的NO或适当缩小容器的体积或增大压强或通入等物质的量的CO2和N2.
15.下列实验结论不正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 某有机物与溴的四氯化碳溶液混合 | 溶液褪色 | 有机物含碳碳双键 |
| B | 乙醇与重铬酸钾(K2Cr2O7)溶液混合 | 橙色溶液变为绿色 | 乙醇具有还原性 |
| C | 常温下,将二氧化碳通入苯酚钠溶液 | 溶液变浑浊 | 酸性:碳酸>苯酚 |
| D | 苯和苯酚稀溶液分别与浓溴水混合 | 后者产生白色沉淀 | 羟基影响了苯环的活性 |
| A. | A | B. | B | C. | C | D. | D |
 .
.
 如图为实验室某浓盐酸试剂瓶标签上的有关数据u,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶标签上的有关数据u,试根据标签上的有关数据回答下列问题: