题目内容
在AB型双核离子化合物中,An+和Bn-两种离子的核外电子数之和为20,可知A、B两元素在元素周期表中其周期的位置是( )
| A、可能都在第2周期 |
| B、若A在第3周期、则B在第4周期 |
| C、可能都在第3周期 |
| D、若A在第3周期、则B在第2周期 |
考点:原子结构与元素的性质,元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:AB型离子化合物中,A元素应为IA、ⅡA族,B元素应为ⅥA、ⅦA族,A、B两种离子的核外电子数之和为20,可以是第二周期的金属和第三周期的非金属,也可以是第三周期的金属和第二周期的非金属,同在第二周期核外电子数之和小于20,同在第三周期核外电子数之和大于20.
解答:
解:A.同在第二周期核外电子数之和小于20,故A错误;
B.若A在第3周期、B在第4周期,则二者核外电子数之和大于20,故B错误;
C.同在第三周期核外电子数之和大于20,故C错误;
D.若A在第3周期、则B在第2周期,其核外电子数之和可能为20,如A是Na元素、B是F元素,故D正确;
故选D.
B.若A在第3周期、B在第4周期,则二者核外电子数之和大于20,故B错误;
C.同在第三周期核外电子数之和大于20,故C错误;
D.若A在第3周期、则B在第2周期,其核外电子数之和可能为20,如A是Na元素、B是F元素,故D正确;
故选D.
点评:本题考查了原子结构和元素性质,明确元素周期表结构、原子结构是解本题关键,根据离子之间的关系解答,题目难度不大.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案
相关题目
向KI溶液中逐滴加入AgNO3溶液,直到沉淀完全为止,生成的溶液的质量与KI溶液的质量相等,则原AgNO3溶液的质量分数约为( 已知:KI+AgNO3=AgI↓+KNO3)( )
| A、72% | B、54% |
| C、46% | D、28% |
我国三峡工程所提供的水电,相当于每年燃烧3000万吨原煤的火力发电站产生的电能,因此三峡工程有助于控制( )
| A、水体污染 | B、白色污染 |
| C、酸雨产生 | D、农药、化肥污染 |
下列离子方程式中正确的是( )
| A、在硫酸铜溶液中加入过量氢氧化钡溶液 Ba2++SO42-=BaSO4↓ |
| B、氯气通入氢氧化钠溶液中 2Cl2+2OH-=3Cl-+ClO-+H2O |
| C、金属钠投入水中 Na+2H2O=Na++2OH-+H2↑ |
| D、稀硫酸和氢氧化钠溶液混合:H++OH-═H2O |
设NA表示阿伏加德罗常数值,下列叙述不正确的是( )
| A、1molO2中含有原子数为2NA个 |
| B、18gH2O中含有原子数为3NA个 |
| C、常温常压下,22.4L H2O中含有的分子数为NA个 |
| D、1L1mol/L Na2SO4溶液中Na+离子数为2NA个 |
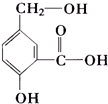 烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题:
烃及烃的含氧衍生物在有机化学中占有举足轻重的地位.请根据相关知识和信息回答下列有关问题: