题目内容
13.下列离子方程式的书写正确的是( )| A. | 铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 氯化铝溶液中加入过量的氨水 Al3++4NH3•H2O=AlO2-+4NH4++2H2 O | |
| C. | 钠和冷水反应 Na+2H2O=Na++2OH-+H2↑ | |
| D. | 纯碱溶液中通入二氧化碳:CO32-+CO2+H2O=2HCO3- |
分析 A.不符合反应客观事实,二者反应生成亚铁离子;
B.不符合反应客观事实,二者反应生成氢氧化铝沉淀和氯化铵;
C.电荷不守恒;
D.二者反应生成碳酸氢钠.
解答 解:A.铁和稀硫酸反应,离子方程式:Fe+2H+=Fe2++H2↑,故A错误;
B.氯化铝的溶液中加入过量氨水的离子反应为Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故B错误;
C.钠和冷水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故C错误;
D.纯碱溶液中通入二氧化碳,离子方程式:CO32-+CO2+H2O=2HCO3-,故D正确;
故选:D.
点评 本题离子方程式的书写,明确发生的反应是解答本题的关键,注意离子反应遵循客观事实、遵循原子个数、电荷守恒规律,题目难度不大.

练习册系列答案
相关题目
3.物质的量相同的下列有机物,充分燃烧耗氧量最大的是( )
| A. | C2H2 | B. | C2H6 | C. | C4H6 | D. | C4H8 |
8.根据所学知识,你认为下列叙述正确的是( )
| A. | 同周期元素原子的最外层电子数相同 | |
| B. | 在周期表中,最外层电子数为1的元素都是金属元素 | |
| C. | 在周期表中,第18列元素的化学性质很稳定 | |
| D. | ⅦA族元素容易失去电子 |
18.下列关于SO2的说法中,不正确的是( )
| A. | SO2是硫及某些含硫化合物在空气中燃烧的产物 | |
| B. | SO2具有漂白性,可以使品红溶液褪色 | |
| C. | SO2溶于水后生成H2SO4 | |
| D. | SO2是一种大气污染物 |
5.综合如图判断,下列正确的说法是( )


| A. | 装置I和装置II中负极反应均是Fe-2e-═Fe2+ | |
| B. | 装置I和装置II中正极反应均是O2+4e-+2H2O-═4OH- | |
| C. | 装置I和装置II中盐桥中的阳离子均向右侧烧杯移动 | |
| D. | 装置I和装置II中正极均被保护 |
9.下列化学用语表示正确的是( )
| A. | 甲烷的比例模型: | B. | 乙烯的结构简式:CH2CH2 | ||
| C. | 氯化氢的电子式: | D. | S2-的结构示意图: |
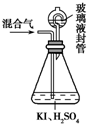 用如图装置可以测定混合气中ClO2的含量:
用如图装置可以测定混合气中ClO2的含量:
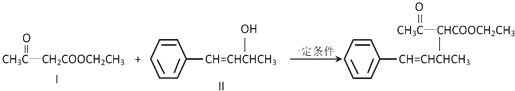
 .
.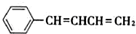 .
.