题目内容
下列物质的水溶液,其pH大于7的是( )
| A、Na2CO3 |
| B、HCl |
| C、Na2SO4 |
| D、KNO3 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:物质的水溶液pH>7,说明该物质是碱或强碱弱酸盐,碱电离出氢氧根离子或强碱弱酸盐水解导致溶液呈碱性.
解答:
解:A.碳酸钠属于强碱弱酸盐,碳酸根离子水解导致溶液中氢氧根离子浓度大于氢离子浓度,所以溶液呈碱性,故A正确;
B.HCl在水溶液里电离出氢离子而使溶液呈酸性,故B错误;
C.硫酸钠是强碱强酸盐,没有水解的离子,所以其溶液呈中性,故C错误;
D.硝酸钾属于强碱强酸盐,没有水解的离子,所以其溶液呈中性,故D错误;
故选A.
B.HCl在水溶液里电离出氢离子而使溶液呈酸性,故B错误;
C.硫酸钠是强碱强酸盐,没有水解的离子,所以其溶液呈中性,故C错误;
D.硝酸钾属于强碱强酸盐,没有水解的离子,所以其溶液呈中性,故D错误;
故选A.
点评:本题考查了溶液酸碱性的判断,根据盐的性质结合“谁强谁显性、谁弱谁水解、强强显中性”来确定电解质溶液的酸碱性,题目难度不大.

练习册系列答案
相关题目
已知2H2O2═2H2O+O2↑,若其他条件不变,下列措施不能使该反应速率增大的是( )
| A、降低温度 |
| B、加入少量MnO2 |
| C、加入少量FeCl3 |
| D、增大H2O2的浓度 |
在2A(g)+B(g)=3C(g)+4D(g)中,下列情况能够降低该反应速率的是( )
| A、增大压强 | B、降低温度 |
| C、使用催化剂 | D、增大A的浓度 |

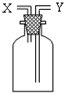 如图所示的装置在实验室中用途比较广泛.
如图所示的装置在实验室中用途比较广泛.




 的化合物称为二肽,二肽还可以继续与其它的α-氨基酸分子脱水形成三肽、四肽以致生成长链的多肽.若丙氨酸[CH3CH(NH2)COOH]与甘氨酸[H2N-CH2-COOH]的混合物在一定条件下反应,可形成二肽的种类有( )
的化合物称为二肽,二肽还可以继续与其它的α-氨基酸分子脱水形成三肽、四肽以致生成长链的多肽.若丙氨酸[CH3CH(NH2)COOH]与甘氨酸[H2N-CH2-COOH]的混合物在一定条件下反应,可形成二肽的种类有( )