题目内容
(15分)I2O5是白色固体,遇水生成碘酸(HIO3)。I2O5可用于检验并定量测定空气中的CO,在常温下发生的反应为 5CO+I2O5=5CO2+I2 (空气中其余气体不与I2O5反应)。
实验一:制取I2O5
将碘酸加热至90~110 ?C使其部分脱水,再升温至220~240 ℃并恒温4 h,使反应完全。接着慢慢冷却至室温,密封保存,即得五氧化二碘。
(1)写出碘酸制I2O5的化学方程式: 。
(2)在制得的I2O5固体中含有少量I2杂质,提纯的方法是 (填标号);
A.过滤 B.蒸发结晶 C.蒸馏 D.升华
用提纯方法用到的玻璃仪器为 (填标号)。
A.圆底烧瓶 B.烧杯 C.普通漏斗 D.酒精灯 E.玻璃棒
实验二:检验空气中CO
利用下图装置检验空气中是否存在CO。
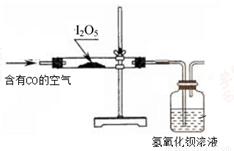
(3)能说明空气中含有CO的现象是 。
(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,请写出改进的实验方案: 。
实验三:测定空气中CO的含量
(5)将I2O5与CO反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗v mL c mol·L-1 Na2S2O3溶液。则该空气样品中CO的体积分数是 。
(6)该实验测定出来的结果不可信,最大可能的原因是: 。
(15分)(1)2HIO3 I2O5+H2O(2分) ;(2)D (2分) A 、B、 D(3分) ;
I2O5+H2O(2分) ;(2)D (2分) A 、B、 D(3分) ;
(3)玻璃管中白色固体变为紫黑色(2分)
(4)空气进入硬质玻璃管之前,先依次通入装有氢氧化钠溶液、浓硫酸的洗气瓶(2分)
(5) 56cv/a(2分);(6)缺少平行实验 (2分)。
【解析】
试题分析:(1)根据题意可得碘酸制I2O5的化学方程式是:2HIO3 I2O5+H2O;(2)在制得的I2O5固体中含有少量I2杂质,为了除去杂质,可以利用I2加热不经过液态就直接变为气态的性质——即升华的性质进行提纯。因此选项是D。用升华这种提纯方法用到的玻璃仪器为圆底烧瓶、烧杯、酒精灯故选项是A、B、D;(3)若空气中含有CO则将空气通入含有I2O5的灼热的硬质玻璃管中,会看到玻璃管中白色固体变为紫黑色;即产生了I2;(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,则改进的实验方案是空气进入硬质玻璃管之前,先依次通入装有氢氧化钠溶液来除去空气中的CO2;再通过盛有浓硫酸的洗气瓶来除去空气中的水蒸气,然后再进行检验;(5)根据方程式5CO+I2O5=5CO2+I2;I2+2Na2S2O3=Na2S4O6+2NaI;可得关系式:5CO~2Na2S2O3;n(Na2S2O3)= v ×10-3L ×c mol/L= cv ×10-3 mol,n(CO)= 5/2 cv ×10-3 mol;V(CO)= 5/2 cv ×10-3 mol×22.4L/mol=56 cv ×10-3L=56 cvml; 则该空气样品中CO的体积分数是V(CO)÷V(空气)=( 56 cvml÷aml)= 56cv/a。(6)由于每一次实验都有偶然性,所以为了使测定数值接近真实值,应该继续多次实验,去平均数值。故该实验测定出来的结果不可信,最大可能的原因是缺少平行实验。
I2O5+H2O;(2)在制得的I2O5固体中含有少量I2杂质,为了除去杂质,可以利用I2加热不经过液态就直接变为气态的性质——即升华的性质进行提纯。因此选项是D。用升华这种提纯方法用到的玻璃仪器为圆底烧瓶、烧杯、酒精灯故选项是A、B、D;(3)若空气中含有CO则将空气通入含有I2O5的灼热的硬质玻璃管中,会看到玻璃管中白色固体变为紫黑色;即产生了I2;(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,则改进的实验方案是空气进入硬质玻璃管之前,先依次通入装有氢氧化钠溶液来除去空气中的CO2;再通过盛有浓硫酸的洗气瓶来除去空气中的水蒸气,然后再进行检验;(5)根据方程式5CO+I2O5=5CO2+I2;I2+2Na2S2O3=Na2S4O6+2NaI;可得关系式:5CO~2Na2S2O3;n(Na2S2O3)= v ×10-3L ×c mol/L= cv ×10-3 mol,n(CO)= 5/2 cv ×10-3 mol;V(CO)= 5/2 cv ×10-3 mol×22.4L/mol=56 cv ×10-3L=56 cvml; 则该空气样品中CO的体积分数是V(CO)÷V(空气)=( 56 cvml÷aml)= 56cv/a。(6)由于每一次实验都有偶然性,所以为了使测定数值接近真实值,应该继续多次实验,去平均数值。故该实验测定出来的结果不可信,最大可能的原因是缺少平行实验。
考点:考查I2O5的制取、分离提纯、实验操作步骤、纯度的计算及误差分析的知识。

 阶梯计算系列答案
阶梯计算系列答案



