题目内容
18.下列电离方程式错误的是( )| A. | KHCO3═K++H++CO32- | B. | NaHSO4═Na++H++SO42- | ||
| C. | KClO3═K++ClO3- | D. | Ba(OH)2═Ba2++2OH- |
分析 A.碳酸氢根离子属于弱酸阴离子,存在电离平衡,不能拆成离子;
B.硫酸氢钠溶液中完全电离生成氢离子、钠离子、硫酸根离子;
C.氯酸钾是盐水溶液中完全电离生成钾离子和氯酸根离子;
D.氢氧化钡是强碱,水溶液中完全电离是钡离子和氢氧根离子.
解答 解:A.碳酸氢根离子属于弱酸阴离子,存在电离平衡,不能拆成离子,电离方程式KHCO3═K++HCO3-,故A错误;
B.硫酸氢钠溶液中完全电离生成氢离子、钠离子、硫酸根离子,电离方程式NaHSO4═Na++H++SO42-,故B正确;
C.氯酸钾是盐水溶液中完全电离生成钾离子和氯酸根离子,电离方程式KClO3═K++ClO3-,故C正确;
D.氢氧化钡是强碱,水溶液中完全电离是钡离子和氢氧根离子,电离方程式Ba(OH)2═Ba2++2OH-,故D正确;
故选A.
点评 本题考查了电离方程式的书写方法和正误判断,注意弱酸阴离子的电离平衡分析,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列用水就能鉴别的一组物质是( )
| A. | 苯、乙醇、四氯化碳 | B. | 苯、己烷、四氯化碳 | ||
| C. | 硝基苯、乙醇、四氯化碳 | D. | 硝基苯、乙醇、乙酸 |
9.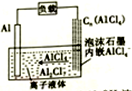 最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
 最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )
最近报道的一种能快速充放电的离子电池,其中的电解质为离子液体{AlCl4-/[EMI]+},放电时有关离子转化如图所示.下列说法正确的是 ( )| A. | 放电时,负极发生2AlCl4--e-═Al2Cl7-+Cl- | |
| B. | 放电时,有机阳离子[EMI]+向铝电极方向移动 | |
| C. | 充电时,阴极发生:4Al2Cl7-+3e-═Al+7AlCl4- | |
| D. | 充电时,泡沫石墨极与外电源的负极相连 |
13.下列说法不正确的是( )
| A. | 用加热法可除去Na2CO3中的NaHCO3 | |
| B. | 硝酸酸化的硝酸银溶液检验Cl- | |
| C. | 可用石灰水区分Na2CO3与NaHCO3溶液 | |
| D. | 热纯碱溶液可除去油污 |
3.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1molCl2常温下与过量稀NaOH溶液反应转移电子总数为0.1NA | |
| B. | 25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | 标准状况下,22.4LCHCl3含有的分子数为NA | |
| D. | 1L 0.1mol•L-1的硫化钠溶液中硫离子数目为0.1NA |
10.以下反应最符合绿色化学原子经济性要求的是( )
| A. | 乙烷与氯气制备一氯乙烷 | |
| B. | 在FeBr3催化作用下,苯与液溴反应制取溴苯 | |
| C. | 苯和硝酸反应制备硝基苯 | |
| D. | 乙烯与氧气在银催化作用下生成环氧乙烷 |
7.仪器可以不直接加热的是( )
| A. | 试管 | B. | 坩埚 | C. | 蒸发皿 | D. | 蒸馏焼瓶 |
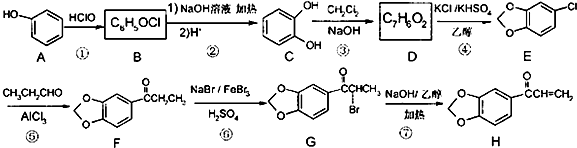
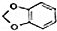
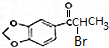 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaBr+H2O
+NaBr+H2O (写出其中一种的结构简式).
(写出其中一种的结构简式).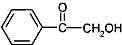 的合成路线.
的合成路线.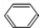 $→_{△}^{Cl_{2}}$
$→_{△}^{Cl_{2}}$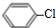 $→_{AlCl_{3}}^{CH_{3}CHO}$
$→_{AlCl_{3}}^{CH_{3}CHO}$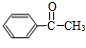 $→_{H_{2}SO_{4}}^{NaBr/FeBr_{2}}$
$→_{H_{2}SO_{4}}^{NaBr/FeBr_{2}}$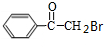 $→_{△}^{NaOH水溶液}$
$→_{△}^{NaOH水溶液}$ .
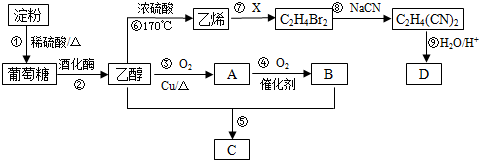
.
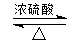 CH3COOCH2CH3+H2O.
CH3COOCH2CH3+H2O.