题目内容
实验室需要配制0.5mol?L-1的烧碱溶液480mL,根据溶液配制的过程,回答下列问题:
(1)实验中除了托盘天平(带砝码)、药匙、烧杯、量筒和玻璃棒外,还需要的其他玻璃仪器有: .
(2)根据计算得知,所需NaOH固体的质量为 g.
(3)配制溶液的过程中,有以下操作,其中正确的是 (填代号).
A.将氢氧化钠固体放在纸片上称量;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中.
(4)玻璃棒在该实验中的作用有:① ,② .
(1)实验中除了托盘天平(带砝码)、药匙、烧杯、量筒和玻璃棒外,还需要的其他玻璃仪器有:
(2)根据计算得知,所需NaOH固体的质量为
(3)配制溶液的过程中,有以下操作,其中正确的是
A.将氢氧化钠固体放在纸片上称量;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;
C.将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中.
(4)玻璃棒在该实验中的作用有:①
考点:溶液的配制
专题:实验题
分析:(1)根据配制一定物质的量浓度的溶液步骤选用仪器,然后判断还缺少的仪器;
(2)实验室没有480mL的容量瓶,需要选用500mL的容量瓶,根据m=nM计算出500mL 0.5mol/L的氢氧化钠溶液中含有氢氧化钠的质量;
(3)根据配制氢氧化钠溶液的正确操作方法进行判断;
(4)配制过程中,溶解氢氧化钠固体需要使用玻璃棒搅拌,转移溶液时需要使用玻璃棒引流.
(2)实验室没有480mL的容量瓶,需要选用500mL的容量瓶,根据m=nM计算出500mL 0.5mol/L的氢氧化钠溶液中含有氢氧化钠的质量;
(3)根据配制氢氧化钠溶液的正确操作方法进行判断;
(4)配制过程中,溶解氢氧化钠固体需要使用玻璃棒搅拌,转移溶液时需要使用玻璃棒引流.
解答:
解:(1)没有规格为480mL的容量瓶,配制时需要选用500mL的容量瓶,实际上配制的是500mL 0.5mol/L的氢氧化钠溶液,配制步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,需要使用的仪器有:托盘天平、玻璃棒、烧杯、药匙、500mL容量瓶、胶头滴管等,还缺少的玻璃仪器为:500mL容量瓶、胶头滴管,
故答案为:500mL容量瓶;胶头滴管;
(2)配制500mL 0.5mol/L的氢氧化钠溶液,需要氢氧化钠的质量为:m(NaOH)=40g/mol×0.5mol/L×0.5L=10.0g,
故答案为:10.0;
(3)A.将氢氧化钠固体放在纸片上称量;氢氧化钠具有较强腐蚀性、易潮解,应该放在烧杯中称量,故A错误;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;氢氧化钠固体在溶解过程中会放出热量,应该冷却后再转移到容量瓶中,否则会导致配制的溶液浓度偏高,故B错误;
C.烧杯和玻璃棒上会粘有部分溶质,所以配制过程中应该将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中,故C正确;
故答案为:C;
(4)配制过程中,溶解氢氧化钠固体时,需要使用玻璃棒搅拌,加速氢氧化钠固体的溶解;转移溶液时,为了避免溶液流到容量瓶以外,应该使用玻璃棒引流,
故答案为:搅拌,加速氢氧化钠固体的溶解;引流.
故答案为:500mL容量瓶;胶头滴管;
(2)配制500mL 0.5mol/L的氢氧化钠溶液,需要氢氧化钠的质量为:m(NaOH)=40g/mol×0.5mol/L×0.5L=10.0g,
故答案为:10.0;
(3)A.将氢氧化钠固体放在纸片上称量;氢氧化钠具有较强腐蚀性、易潮解,应该放在烧杯中称量,故A错误;
B.在烧杯中溶解氢氧化钠固体后,立即将溶液倒入容量瓶中;氢氧化钠固体在溶解过程中会放出热量,应该冷却后再转移到容量瓶中,否则会导致配制的溶液浓度偏高,故B错误;
C.烧杯和玻璃棒上会粘有部分溶质,所以配制过程中应该将溶解氢氧化钠的烧杯用蒸馏水洗涤2~3次,并将洗涤液转移到容量瓶中,故C正确;
故答案为:C;
(4)配制过程中,溶解氢氧化钠固体时,需要使用玻璃棒搅拌,加速氢氧化钠固体的溶解;转移溶液时,为了避免溶液流到容量瓶以外,应该使用玻璃棒引流,
故答案为:搅拌,加速氢氧化钠固体的溶解;引流.
点评:本题考查了配制一定物质的量浓度的溶液的方法,该题是中等难度的试题,试题基础性强,贴近高考;该题难易适中,注重灵活性,侧重对学生能力的培养和解题方法的指导和训练,有利于培养学生的逻辑思维能力和严谨的规范实验操作能力.

练习册系列答案
相关题目
下列物质按照纯净物、混合物、电解质和非电解质顺序排列的是( )
| A、盐酸、水煤气、醋酸、干冰 |
| B、单甘油酯、混甘油酯、苛性钠、氨气 |
| C、冰醋酸、福尔马林、硫酸钠、乙醇 |
| D、胆矾、漂白粉、氯化钾、氯气 |
实验中需2mol?L-1的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A、500 mL,106g |
| B、950 mL,201.4g |
| C、任意规格,201.4g |
| D、1000 mL,212g |
下列各组离子,在强酸性溶液中可以大量共存的是( )
| A、K+、Fe2+、SO42-、Br- |
| B、Na+、Al(OH)4-、Cl-、SO42- |
| C、Mg2+、Ca2+、HCO3-、Cl- |
| D、Fe2+、Ca2+、Cl-、NO3- |
火箭新兵“长三丙火箭”第三级推进器使用的燃料是液态氢,已知在298K时,2g H2与O2完全反应生成液态水时放热285.8kJ.则下列有关判断正确的是( )
| A、在298 K时,11.2 L H2完全燃烧生成液态水放出的热量为142.9 kJ | ||
| B、H2(g)的燃烧热是285.8 kJ,则2H2O(l)═2H2(g)+O2(g)△H=+571.6 kJ?mol-1 | ||
| C、在298 K时,2H2(g)+O2(g)═2H2O(g)△H<-571.6 kJ?mol-1 | ||
D、H2(g)+
|
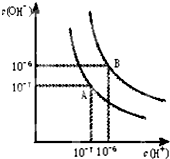 (1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
(1)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),