题目内容
将4mol A气体和2mol B气体在2L的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)═2C(g),反应2min的时间,并测得该段时间内C的反应速率为0.6mol?L-1?min-1,现有下列几种说法中正确的是( )
①用物质A表示的反应的平均速率为0.6mol?L-1?s-1
②用物质B表示的反应的平均速率为0.05mol?L-1?s-1
③2min时容器中A的物质的量为2.8mol
④2min时物质B的浓度为0.4mol?L-1.
①用物质A表示的反应的平均速率为0.6mol?L-1?s-1
②用物质B表示的反应的平均速率为0.05mol?L-1?s-1
③2min时容器中A的物质的量为2.8mol
④2min时物质B的浓度为0.4mol?L-1.
| A、①③ | B、②④ | C、②③ | D、④ |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:①根据不同物质表示的速率之比等于其化学计量数之比计算v(A);
②根据不同物质表示的速率之比等于其化学计量数之比计算v(B);
③根据v=
进行公式变形计算△n(A),2min时A的物质的量等于A的起始物质的量减去△n(A);
④根据v=
进行公式变形计算△c(B),2min时B的浓度等于B的起始浓度减去△c(B).
②根据不同物质表示的速率之比等于其化学计量数之比计算v(B);
③根据v=
| ||
| △t |
④根据v=
| △c |
| △t |
解答:
解:对于反应:2A(g)+B(g)═2C(g),反应2min的时间,并测得该段时间内C的反应速率为0.6mol?L-1?min-1,
①不同物质表示的速率之比等于其化学计量数之比,则v(A)=v(C)=0.6mol?L-1?min-1=0.01mol?L-1?s-1,故①错误;
②不同物质表示的速率之比等于其化学计量数之比,则v(B)=
v(C)=0.3mol?L-1?min-1=0.005mol?L-1?s-1,故②错误;
③根据v=
可知,△n(A)=0.6mol?L-1?min-1×2min×2L=2.4mol,故2min时A的物质的量为4mol-2.4mol=1.6mol,故③错误;
④根据v=
可知,△c(B)=0.3mol?L-1?min-1×2min=0.6mol/L,故2min时B的浓度为
-0.6mol/L=0.4mol/L,故④正确,
故选D.
①不同物质表示的速率之比等于其化学计量数之比,则v(A)=v(C)=0.6mol?L-1?min-1=0.01mol?L-1?s-1,故①错误;
②不同物质表示的速率之比等于其化学计量数之比,则v(B)=
| 1 |
| 2 |
③根据v=
| ||
| △t |
④根据v=
| △c |
| △t |
| 2mol |
| 2L |
故选D.
点评:本题考查化学反应速率的有关计算,难度不大,注意对公式的理解与灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列分散系中分散质粒子最大的是( )
| A、蔗糖溶液 |
| B、少量植物油和水的混合物 |
| C、牛奶 |
| D、硫酸溶液 |
下列各组有机物中,不论二者以什么比例混合,只要总质量一定,则完全燃烧时消耗O2的质量和生成水的质量不变的是( )
| A、CH4 C2H6 |
| B、C2H6 C3H6 |
| C、C2H4 C3H6 |
| D、C3H4 C3H6 |
某气体混合物由H2、N2、CO和CH4中的一种或两种组成,将该混合气体点燃后的产物依次通过浓H2SO4和NaOH溶液,结果两溶液的质量均有增加.则该混合气体的组成不可能是( )
| A、N2和CO |
| B、H2和CO |
| C、CH4 |
| D、H2和CH4 |
 Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空:
Ⅰ.粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成;请填空: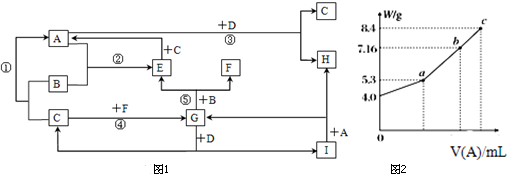
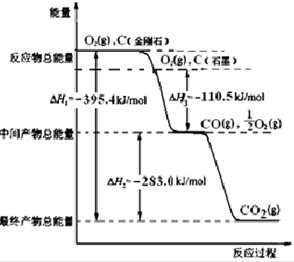 能源危机是当前全球问题,开源节流是应对能源危机的重要举措.
能源危机是当前全球问题,开源节流是应对能源危机的重要举措.