题目内容
17.Ⅰ.对某星球外层空间取回的气体样品分析如下:①将样品溶于水,发现其主要成分气体A极易溶于水,水溶液呈酸性;
②将A的浓溶液与KMnO4反应产生一种黄色气体单质B,将B通入石灰乳可生成两种钙盐的混合物D;
③A的稀溶液与锌粒反应生成气体C,C和B的气体充分混合经光照发生爆炸又生成气体A,实验测得反应前后气体体积不变.
据此回答下列问题:
(1)化学式:AHCl;CH2;
(2)气体B与Ca(OH)2反应的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
Ⅱ.双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN,其中N元素表现为-3价),化学方程式为:KCN+H2O+H2O2=KHCO3+A↑(已配平)
(3)生成物A的化学式为NH3,该反应中的氧化剂H2O2;
(4)若将KCN改为HCN也类似上述反应,则该反应的化学方程式为HCN+H2O2=CO2↑+NH3↑.
分析 Ⅰ.A极易溶于水,水溶液呈酸性,将A的浓溶液与KMnO4共热,生成一种黄绿色单质气体B,则A为HCl,B为Cl2,将B通入石灰乳可生成两种钙盐的混合物D,则D为CaCl2、Ca(ClO)2,A的稀溶液与锌粒反应生成气体C,C和B的气体充分混合经光照发生爆炸又生成气体A,则C为H2,以此来解答.
Ⅱ.(3)依据化学方程式为KCN+H2O2+H2O=KHCO3+A↑,结合原子个数守恒判断A的化学式,根据化合价的变化判断氧化剂;
(4)若将KCN改为HCN也发生类似上述反应,则产物应为CO2和NH3.
解答 解:Ⅰ.A极易溶于水,水溶液呈酸性,将A的浓溶液与KMnO4共热,生成一种黄绿色单质气体B,则A为HCl,B为Cl2,将B通入石灰乳可生成两种钙盐的混合物D,则D为CaCl2、Ca(ClO)2,A的稀溶液与锌粒反应生成气体C,C和B的气体充分混合经光照发生爆炸又生成气体A,则C为H2,
(1)根据上面的分析可知,A为HCl,C为H2,
故答案为:HCl;H2;
(2)B为Cl2,B与Ca(OH)2反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,
故答案为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O;
Ⅱ.(3)依据化学方程式为:KCN+H2O2+H2O=KHCO3+A↑,由原子个数守恒可知:A中有1个氮原子和3个氢原子,为NH3,在反应中,H2O2中的氧从-1价降为-2价,是氧化剂,
故答案为:NH3; H2O2;
(4)若将KCN改为HCN也发生类似上述反应,则产物应为CO2和NH3,方程式为HCN+H2O2=CO2↑+NH3↑,
故答案为:HCN+H2O2=CO2↑+NH3↑.
点评 本题考查了查氧化还原反应,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,解答本题注意从质量守恒的角度判断生成物,题目难度中等.

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案| A. | 均不能与酸反应 | B. | 均能与水直接化合生成酸 | ||
| C. | 能与碱反应生成盐和水 | D. | 不可能是金属氧化物 |
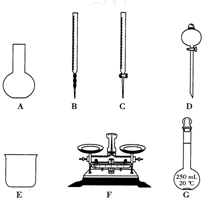
| A. | 试管 | B. | 烧瓶 | C. | 量筒 | D. | 烧杯 |
| A. | 滴有碘水的淀粉溶液10ml分成两等份于两支试管,分别加入稀硫酸和唾液1ml,振荡,前者褪色快 | |
| B. | 恒温下,将盛有NO2和N2O4的平衡体系加压,体系颜色最终变浅 | |
| C. | 草酸溶液与酸性KMnO4溶液混合后,由于生成物对反应有催化作用,会使反应速率加快 | |
| D. | 在K2Cr2O7溶液中滴加浓硫酸,溶液颜色由橙色变黄色 |
| A. | CS2和SO3 | B. | P4和CH4 | C. | NH3和H2S | D. | CCl4和C2H4 |
 某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…