题目内容
2SO2(g)+O2(g)
2SO2(g)是制备硫酸的重要反应.下列叙述正确的是( )
| V2O5 |
| △ |
| A、催化剂V2O5不改变该反应的逆反应速率 | ||
B、在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=
| ||
| C、该反应是放热反应,降低温度将缩短反应达到平衡的时间 | ||
| D、以上说法均不合理 |
考点:化学平衡的调控作用
专题:化学平衡专题
分析:根据催化剂可以同等程度的增大正逆反应的反应速率;降低温度反应速率减小及化学反应速率v=
的计算式来解答.
| △c |
| △t |
解答:
解:A、催化剂可同等程度的改变正、逆反应的反应速率,故A错误;
B、根据计算平均速率的定义公式,浓度变化量c2-c1,时间为t2-t1,SO3(g)生成的平均速率为v=
,故B正确;
C、不论反应是吸热反应还是放热反应,降低温度反应速率一定变慢,则达到平衡的时间将延长,故C错误;
D、因为B正确,故D错误;
故选B.
B、根据计算平均速率的定义公式,浓度变化量c2-c1,时间为t2-t1,SO3(g)生成的平均速率为v=
| c2-c1 |
| t2-t1 |
C、不论反应是吸热反应还是放热反应,降低温度反应速率一定变慢,则达到平衡的时间将延长,故C错误;
D、因为B正确,故D错误;
故选B.
点评:本题主要考查了影响化学反应速率的因素,化学反应速率和化学平衡是化学基本理论的核心知识,既是重点又是难点,也是年年必考的内容,特别是有关化学反应速率和化学平衡的计算及影响因素、化学平衡常数的表达式及其计算是高考的重点.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列关于NO、NO2的说法中,错误的是( )
| A、NO2是红棕色气体 |
| B、NO2有刺激性气味 |
| C、NO是黄绿色气体 |
| D、NO能与血红蛋白结合,有毒 |
经研究发现,有一种磷分子具有链状结构,其结构简式为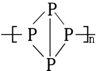 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、它是一种高分子化合物 |
| B、它的分子中具有极性共价键 |
| C、分子中每个磷原子以三个共价健分别结合三个磷原子 |
| D、分子中具有不饱和键 |
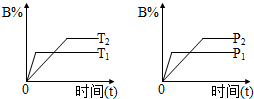 某可逆反应:mA(g)+nB(g)?pC(g);在密闭容器中进行,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )
某可逆反应:mA(g)+nB(g)?pC(g);在密闭容器中进行,如图所示,反应在不同时间t、温度T和压强p与反应物B在混合气体中的百分含量(B%)的关系曲线,由曲线分析下列判断正确的是( )| A、T1<T2,p1>p2,n+m>p,(正反应为吸热反应) |
| B、T1>T2,p1>p2,n+m>p,(正反应为吸热反应) |
| C、T1>T2,p1>p2,n+m<p,(正反应为吸热反应) |
| D、T1>T2,p1>p2,n+m>p,(正反应为放热反应) |
在下列结构的有机化合物中:属于同分异构体的正确组合是( )
①CH3-CH2-CH2-CH2-CH3
②CH3-CH2-CH2-CH2-CH2-CH3
③
④
⑤
①CH3-CH2-CH2-CH2-CH3
②CH3-CH2-CH2-CH2-CH2-CH3
③

④

⑤

| A、①和③ | B、②、③和⑤ |
| C、①和② | D、④和③ |
含3.01×1022个氢原子的水物质的量是( )
| A、3.01×1022mol |
| B、0.5mol |
| C、0.05mol |
| D、0.025mol |
下列叙述中,正确的是( )
| A、二氧化硫的摩尔质量是64g | ||
| B、一个镁的原子质量就是镁的相对原子质量 | ||
| C、水的相对分子质量等于18g | ||
D、一个16O的实际质量约等于
|
下列各组物质的溶液,两者相互滴加现象不同的是( )
| A、FeCl3和NaOH |
| B、NaHCO3和HCl |
| C、NaAlO2和HCl |
| D、AlCl3和NH3?H2O |