题目内容
经研究发现,有一种磷分子具有链状结构,其结构简式为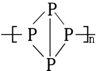 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A、它是一种高分子化合物 |
| B、它的分子中具有极性共价键 |
| C、分子中每个磷原子以三个共价健分别结合三个磷原子 |
| D、分子中具有不饱和键 |
考点:晶体的类型与物质的性质的相互关系及应用
专题:化学键与晶体结构
分析:A、该物质为磷元素组成的单质;
B、该分子中的化学键均为P-P键,为非极性键;
C、该分子中每个P与相邻的P均形成三条P-P键;
D、该分子中的化学键均为P-P键,不含不饱和键.
B、该分子中的化学键均为P-P键,为非极性键;
C、该分子中每个P与相邻的P均形成三条P-P键;
D、该分子中的化学键均为P-P键,不含不饱和键.
解答:
解:A、该物质为磷元素组成的单质,不是化合物,故A错误;
B、该分子中的化学键均为P-P键,为非极性键,故B错误;
C、该分子中每个P与相邻的P均形成三条P-P键,故C正确;
D、该分子中的化学键均为P-P键,不含不饱和键,故D错误;
故选C.
B、该分子中的化学键均为P-P键,为非极性键,故B错误;
C、该分子中每个P与相邻的P均形成三条P-P键,故C正确;
D、该分子中的化学键均为P-P键,不含不饱和键,故D错误;
故选C.
点评:本题考查了分子晶体的组成、化学键类型、饱和度等知识,题目难度不大,注意共价键中极性键和非极性键的区别.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
下列关于物质的用途中叙述正确的是( )
| A、Fe3O4常用作红色油漆和涂料 |
| B、氧化铝(Al2O3)可用于制造耐火材料 |
| C、明矾(KAl(SO4)2?12H2O)可用作净水剂 |
| D、NaOH可用作胃酸中和剂 |
将32.2g Na2SO4?10H2O溶于水配成500mL溶液,取出其中1/10的溶液,其溶液的物质的量浓度为( )
| A、0.1 mol/L |
| B、0.2 mol/L |
| C、0.3 mol/L |
| D、0.4 mol/L |
下列关于稀有气体的叙述不正确的是( )
| A、原子的最外电子数都有8个电子 |
| B、其原子与下一周期IA、IIA族阳离子具有相同的核外电子排布 |
| C、化学性质非常不活泼 |
| D、不能形成双原子分子 |
下列说法或做法正确的是( )
| A、黑色金属材料通常包括铁、铬、锰以及它们的合金 |
| B、镁在空气中燃烧的产物只有MgO |
| C、海水提镁和海水提溴所涉及的化学反应全都是氧化还原反应 |
| D、用量筒量取10.0mL1.0mol?L-1 的盐酸于100mL容量瓶中,加水稀释至刻度,可制得0.1mol?L-1 的盐酸 |
通过一步反应不能直接完成的是( )
(1)N2→NO2(2)S→SO2 (3)NH3→NO(4)NO→HNO3(5)CuSO4→Cu(NO3)2(6)SiO2→H2SiO3.
(1)N2→NO2(2)S→SO2 (3)NH3→NO(4)NO→HNO3(5)CuSO4→Cu(NO3)2(6)SiO2→H2SiO3.
| A、(1)(6) |
| B、(4)(5) |
| C、(1)(4)(6) |
| D、(5)(6) |
氯水中存在如下平衡:Cl2+H2O?H++Cl-+HClO,为了增强漂白效果,可向氯水中加入的物质是( )
| A、CaCO3 |
| B、NaOH |
| C、NaCl溶液 |
| D、FeCl2溶液 |
2SO2(g)+O2(g)
2SO2(g)是制备硫酸的重要反应.下列叙述正确的是( )
| V2O5 |
| △ |
| A、催化剂V2O5不改变该反应的逆反应速率 | ||
B、在t1、t2时刻,SO3(g)的浓度分别是c1、c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=
| ||
| C、该反应是放热反应,降低温度将缩短反应达到平衡的时间 | ||
| D、以上说法均不合理 |
丙烯酸酯CH2=CHCOOR不能发生的化学反应是( )
| A、加成反应 | B、加聚反应 |
| C、酯化反应 | D、氧化反应 |